Как уже указывалось, во всех биокосных системах (сегодня крупнейшей из них является биосфера) живое и косное вещество неразрывно связаны и обусловлены друг другом. Именно это позволяет относить состав косного вещества, а также поведение химических элементов в каждой из рассмотренных геохимических систем к числу основных факторов, существенно воздействующих на организмы и определяющих условия их развития. Именно от этих факторов в значительной мере зависит безопасность жизнедеятельности людей.
45
До последнего времени поведение химических элементов в среде обитания живого вещества (т.е. в различных геохимических системах) характеризовалось двумя основными показателями: распространенностью (содержанием) химических элементов и формой их нахождения. К ним целесообразно присоединить третий показатель – распределение элементов в конкретной крупной геохимической системе (В. А. Алексеенко, 1997). Рассмотрим несколько подробнее эти три показателя и их вероятную связь с развитием организмов. Это можно сделать на различных уровнях: для всей биосферы (а соответственно и для всего живого вещества Земли, включая человека) и для отдельных участков биосферы и развивающихся только в их пределах определенных организмов.
Распространенность химических элементов в земной коре. Развитие и существование жизни на Земле несомненно должны определяться распространенностью химических элементов в поверхностных частях земной коры, в пределах которых существуют организмы. Основу этих частей, как и земной коры в целом, составляют горные породы, образующие литосферу. Если рассматривать весь блок живого вещества Земли, то можно считать, что его существование обусловлено особенностями распространенности химических элементов в земной коре в целом. Эти особенности были довольно хорошо изучены такими выдающимися учеными, как В.И. Вернадский, А.Е. Ферсман, В.М. Гольдшмидт, Ф.У. Кларк.
Для характеристики рассматриваемых особенностей часто используется термин "кларк" – среднее содержание определенного элемента в конкретной очень крупной геохимической системе. У нас он обычно выражается в процентах, хотя в западных странах все чаще выражают в млн-1, г/т, млрд-1 (табл. 3.1). Сам термин "кларк" был введен в науку А.Е. Ферсманом в честь Ф.У. Кларка, впервые определившего содержание в земной коре наиболее распространенных элементов.
Первоначально (Ф.У. Кларк, 1889) были определены проценты от массы земной коры для отдельных химических элементов, названные массовыми кларками земной коры (табл. 3.2). Потом было установлено, какой процент занимают объемы атомов определенных химических элементов от общего объема земной коры, а также их числа от общего числа атомов в земной коре, названные (соответственно) объемными и атомными кларками
46
Таблица 3.1
Соотношение между различными единицами измерения
среднего содержания элемента
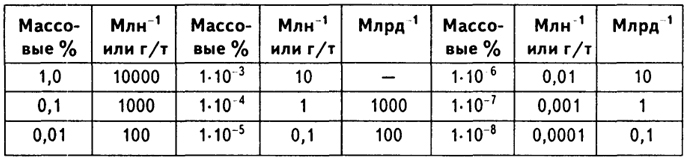
земной коры. Позже были установлены средние содержания химических элементов в различных типах горных пород (кларки горных пород) и в отдельных крупных регионах типа Кавказа или Урала (местные или региональные кларки).
Вернемся к рассмотрению закономерностей распространения химических элементов в различных крупных геохимических системах и в первую очередь в земной коре.
1. Элементы распространены в земной коре крайне неравномерно. Одних из них в миллиард миллиардов раз (от n · 10 до n · 10-16) больше, чем других. На долю только О и Si приходится около 70% массы земной коры. Если к ним добавить еще шесть элементов (Al, Fe, Ca, Mg, К, Na), то их суммарная масса составит около 99% массы коры. Добавив к ним еще 29 наиболее распространенных элементов, получим прибавку всего около 1%, при этом на большую часть (по числу) всех оставшихся элементов будут приходиться лишь сотые доли процентов массы земной коры.
Если учитывать объемы атомов, то рассматриваемая неравномерность станет еще более контрастной.
Многие исследователи группировали химические элементы с учетом их кларкового содержания. Так, иногда породообразующими называются 9 наиболее распространенных в литосфере химических элементов: О, Si, Al, Fe, Ca, К, Na, Mg, Ti. На их долю приходится 99,5 % массы земной коры.
Элементы с массовыми кларками меньше 1·10-2% часто называют редкими. Однако при таком подходе к редким следует относить более 70% химических элементов, известных в земной коре. Ясна бессмысленность
47
Таблица 3.2
Значения абсолютных (АР) и относительных (ОР) разбросов кларковых содержаний химических элементов в магматических породах, в породах континентов и в образованиях океанического дна

48
Примечания: Черта под цифрой символизирует минимальный абсолютный разброс в магматических породах; две черты – максимальный абсолютный разброс в магматических породах и максимальный относительный разброс. В скобках приведены данные без учета содержаний в почвах.
49
такого названия. Но даже уменьшив еще в 100 раз пороговое содержание (до 1·10-4%), придется считать "редкими" более трети элементов. Совершенно иной смысл в это понятие вкладывал И.И. Гинзбург, относивший к редким элементы, редко (мало) используемые человечеством. Приведенные данные указывают на необходимость осторожного подхода к термину "редкие элементы".
Довольно часто употребим (особенно в биогеохимической литературе) и термин "микроэлементы". А.И. Перельман рекомендует (1979) употреблять его только с указанием конкретной природной системы. Так AI – микроэлемент в организмах и макроэлемент в литосфере. За пороговое значение предложено брать 1·10-2%.
2. Для рассмотрения следующей закономерности необходимо привлечение "кривой Ферсмана" – полулогарифмического графика, на котором по оси абсцисс отложены порядковые номера элементов, а по оси ординат – логарифмы атомных кларков. Как видно из рис. 3.1, положение большей части элементов колеблется, не отходя далеко от условной усредняющей (показана сплошной линией). По отношению к усредненному распространению выделяются элементы резко преобладающие – избыточные и с особо малым содержанием – недостаточные.

Рис. 3.1. Логарифмы атомных кларков элементов (по А.Е. Ферсману)
50
К избыточным относятся О, AI, Si, Fe, Ba, Th. Несколько условно к ним иногда причисляют К, Са, РЬ. Объяснить их избыточное распространение какой-либо одной важнейшей причиной пока не удалось. Можно только отметить, что за исключением AI и К все они имеют четные атомные номера, а атомные массы большинства кратны четырем.
К недостаточным относятся резко дефицитные инертные газы (Не, Ne, Кr, Хе, Аr), а также Li, Be, В. Малая распространенность благородных газов объясняется двумя гипотезами. Первая предполагает их постоянный отток от Земли – так называемое гелиевое дыхание Земли. Эта гипотеза более распространена среди геохимиков, начиная с В.И. Вернадского и А.Е. Ферсмана. По второй гипотезе еще при формировании планеты инертные газы оттеснялись от сгущавшихся частиц (как это наблюдается в хвостах планет) и были дефицитными уже на этой стадии. Вполне вероятно, в определенной мере справедливы обе гипотезы.
Низкие кларки Li, Be, В обычно объясняются недостаточной устойчивостью их атомных ядер. Это подтверждается экспериментальными данными.
3. Ведущим химическим элементом земной коры является кислород. Его массовый кларк определяется в пределах 46,28...49%, атомный – 53,3%, а объемный – 92%. Это позволяет считать земную кору кислородной сферой. В биосфере несколько возрастает относительная роль гидросферы, состоящей из Н и О, а в связи с этим еще больше возрастает содержание кислорода. Он же определяет возможность развития подавляющего большинства организмов, а основная часть свободного кислорода в биосфере считается продуктом фотосинтеза.
По имеющимся расчетам (И.Ф. Реймерс, 1990) в настоящее время свободный кислород образуется со скоростью 1,55·109 т/год, а расходуется 2,16·1010 т/год. Таким образом, расход свободного кислорода в ноосфере более чем в 10 раз превышает его образование. Есть над чем задуматься экологам!
Еще одна особенность: в земной коре, 92% объема которой приходится на долю кислорода, преобладают так называемые бескислородные восстановительные обстановки. Это означает, что в большей части литосферы отсутствует свободный кислород. Даже в биосфере встречается довольно много зон с бескислородными глеевой и сероводородной обстановками. Иногда их размеры столь велики, что прорыв в атмосферу H2S из таких зон
51
может стать катастрофой планетарного масштаба. В нашей стране к одной из таких зон относится, например, Прикаспий. Нужно тщательно продумывать свою деятельность (в частности добычу нефти и газа), чтобы не допустить возможности таких прорывов H2S.
4. Возвращаясь к рис. 3.1, отметим, что содержание химических элементов в земной коре неравномерно убывает по мере увеличения их порядковых номеров и атомных масс. Так, из шести элементов, составляющих 98% объема коры, наибольший порядковый номер 20, а наибольшая атомная масса – 40 (Са). О резком преобладании легких элементов свидетельствует и средняя атомная масса земной коры, равная 17,25. Для сравнения вспомним, что атомная масса As равна 74,92, Sr – 87,62, Cd – 112,41, W – 183,8, Hg - 200,5, Pb - 207,2 и U - 238,2.
В биосфере, представляющей верхний слой земной коры с существенной ролью гидросферы и атмосферы, преобладание легких элементов выражено еще более контрастно. Исходя из этого, становятся понятными токсичность тяжелых металлов при их повышенной концентрации и зависимость "биологической важности" элементов от их положения относительно линии питательных веществ (см. дальше).
5. В таблице Д. И. Менделеева элементы с четными порядковыми номерами и с четными атомными массами являются более распространенными, чем рядом расположенные элементы с нечетными номерами. Эта закономерность была установлена итальянцем Г. Оддо и американцем В. Гаркинсом и по их фамилиям получила название Оддо-Гаркинса. Всего же массовые кларки четных элементов составляют в сумме более 86%.
6. Особым преобладанием в земной коре отличаются элементы, атомная масса которых кратна четырем: О (16), Мд (24), Si (28), Са (40). В связи с этим можно предполагать, что если бы не удаление с Земли, то кларки Не(4), Ne(20), Ar(40) были бы несравненно большими.
7. Среди изотопов одного элемента обычно преобладают те, массовое число которых кратно четырем. Особо наглядно это выглядит на примере кислорода и серы:
- 16O – 99,76%
- 17O – 0,04%
- 18O – 0,20%
52
8. У нечетных и четных элементов в начале таблицы Менделеева наибольшие кларки характерны для шестых по порядковому номеру элементов: у нечетных - Н (1), N (7), AI (13), К (19), Мn (25); у четных - О (8), Si (14), Са (20), Fe (26). Объяснения этой закономерности пока нет.
Из рассмотрения закономерностей распространения элементов в земной коре следует, что в ней резко преобладают легкие элементы с четными порядковыми номерами и атомными массами, представленные изотопами типа 4п с устойчивыми ядрами и удерживающиеся гравитационным полем Земли.
Все изложенное позволяет сделать вывод:
Процесс эволюционного развития организмов происходил в среде со всеми известными химическими элементами, некоторые из них (радиоактивные) к настоящему времени в земной коре вымерли. При этом в среде обитания существенно преобладают легкие химические элементы с четными порядковыми номерами и атомными массами, особенно атомная масса которых кратна четырем.
Именно эти условия наиболее благоприятны для безопасной жизнедеятельности.
Рассмотренные особенности распространения химических элементов в земной коре сказались на развитии и составе живых организмов планеты. Так, химические элементы, наиболее необходимые в значительных содержаниях для нормального развития организмов, расположены или непосредственно на "линии жизни" или вблизи от нее. Сама линия жизни (ее еще называют "линией питательных веществ") представляет собой ломаную, соединяющую в таблице Д. И. Менделеева углерод с железом и калием (рис 3.2).
Считается, что чем дальше и ниже от линии жизни расположены элементы таблицы Д.И. Менделеева, тем более опасны они для большинства живых организмов, в том числе и для человека, при высокой концентрации в среде обитания этих организмов. На большинство организмов, также включая человека, отрицательно воздействует недостаток в первую очередь тех элементов, которые расположены в непосредственной близости от линии жизни.
Особенности распространенности химических элементов в земной коре оказали влияние и на химический состав живого вещества. Так, в него входят практически все химические элементы, известные в земной коре. Неравномерность распространения элементов в общей массе живых организмов
53

Рис. 3.2. Линия питательных веществ
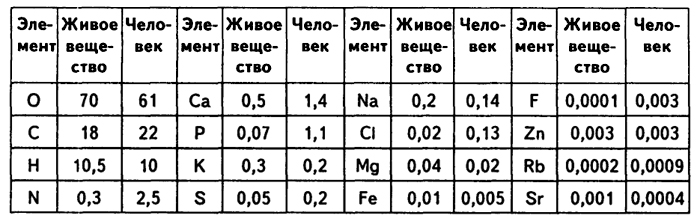
еще более усилилась, и на долю всего трех элементов (О, С, Н) приходится свыше 98% массы живого вещества (табл. 3.3).
Основным элементом в организмах, как и в земной коре, является кислород. Основу живого вещества составляют химические элементы, доминирующий изотоп которых построен по типу 4n (12C, 160, 24Mg, 28Si, 32S, 40Ca, 60Fe). При этом легкие элементы преобладают над тяжелыми. Закономерности, указанные для всей массы живого вещества, справедливы и для человеческого организма (табл. 3.4).
Уже была рассмотрена связь распространения химических элементов в земной коре с химическим составом всего блока живого вещества Земли в целом, а также влияние особенностей этого распространения на условия развития на Земле жизни как таковой. Однако выяснилось, что жизнь и развитие отдельных конкретных видов организмов во многом обусловлены специфическими геохимическими особенностями относительно небольших участков земной коры с преобладанием горных пород определенного типа. К настоящему времени это явление наиболее изучено для растений суши.
Так, по наблюдениям С.М. Ткалича, на Сахалине над угленосными пластами произрастают лиственные ольхово-березовые леса, а над вмещающими их породами – хвойные. В Сибири над кимберлитами на фоне лишайниковых редколесий выделяются лиственнично-ольховые леса. В Иркутской области по изменению состава растительности выделялись площади, занятые магматическими породами – траппами.
54
Таблица 3.3
Среднее содержание химических элементов в живом веществе

Таблица 3.4
Средние процентные содержания в живом веществе планеты
и в человеке наиболее распространенных химических элементов
(по данным J. Emsley, H.J. Bowen, А.И. Перельмана, В.А. Алексеенко)
55
Специфические геохимические особенности регионов несомненно воздействуют и на обитающих в их пределах людей, что особенно видно, если на одном месте проживает несколько поколений их. Это имеет свои плюсы и минусы. Специальные исследования показывают, что среди долгожителей преобладают те, чьи предки долгое время жили в одном регионе и привыкли к данной геохимической обстановке. В то же время, если геохимические особенности региона существенно отличаются от обычных и вышерассмотренных условий, у долго проживающих в нем людей возможно появление специфических заболеваний. Например, район Уров в Сибири выделяется резким избытком Sr и недостатком Са, в его пределах развивается "уровская болезнь", при которой нарушается строение скелета: наблюдаются искривления позвоночника, опухоль суставов, ломкость костей. Аналогичные районы известны в Маньчжурии, в бассейне реки Зеи и в других местах (А. И. Перельман, 1972). Ряд исследователей объясняет причины малорослости населения лесов Центральной Африки, например пигмеев, аномально низким содержанием Са в почвах и продуктах питания. Подобные явления изучены для диких и домашних животных, рыб, птиц.
Из вышесказанного можно сделать следующие выводы:
- Для жизнедеятельности большинства организмов благоприятна распространенность элементов, близкая к кларковой.
- Резко выраженные специфические особенности распространенности ряда элементов в отдельных регионах непосредственно сказываются на здоровье людей, вызывая изменения концентраций этих элементов в растительных и животных организмах, обычно являющихся продуктами питания человека.
- В большинстве случаев при миграции населения нецелесообразно резко менять геохимические условия проживания по сравнению с теми, в которых жили предки. Это может существенно уменьшить безопасность жизнедеятельности переселенцев.
Форма нахождения химических элементов в среде обитания организмов. Состав живого вещества и условия развития жизни на Земле во многом определяются и преобладанием определенных форм нахождения химических элементов в среде обитания организмов. Так, в составе земной коры преобладают химические элементы, для которых предпочтительной является минеральная форма, а организмы поглощают в основном химические
56
элементы, находящиеся в водных растворах, газовых смесях и в биологической форме. Это сказалось и на особенностях химического состава организмов:
- воздушные мигранты составляют в живом веществе свыше 98% его массы, а в земной коре – лишь около 50%;
- среди водных мигрантов (по А.И. Перельману) в организмах преобладают подвижные. На их долю приходится 0,7%, а на долю малоподвижных – около 0,5%. В земной же коре преобладают слабо- и малоподвижные, составляя свыше 44%. На долю подвижных приходится всего около 8%;
- обособленные в пространстве земной коры такие формы нахождения элементов, как минеральная, водные растворы, газовые смеси, коллоидная и сорбированная, в живом веществе часто пространственно совмещены, образуя единый организм.
Как уже указывалось, с учетом форм нахождения химических элементов в составе земной коры при различных экологических исследованиях отдельно выделяются гидросфера, атмосфера, почвы и живое вещество. Все они имеют огромное значение и свою специфику воздействия на безопасность жизнедеятельности людей.
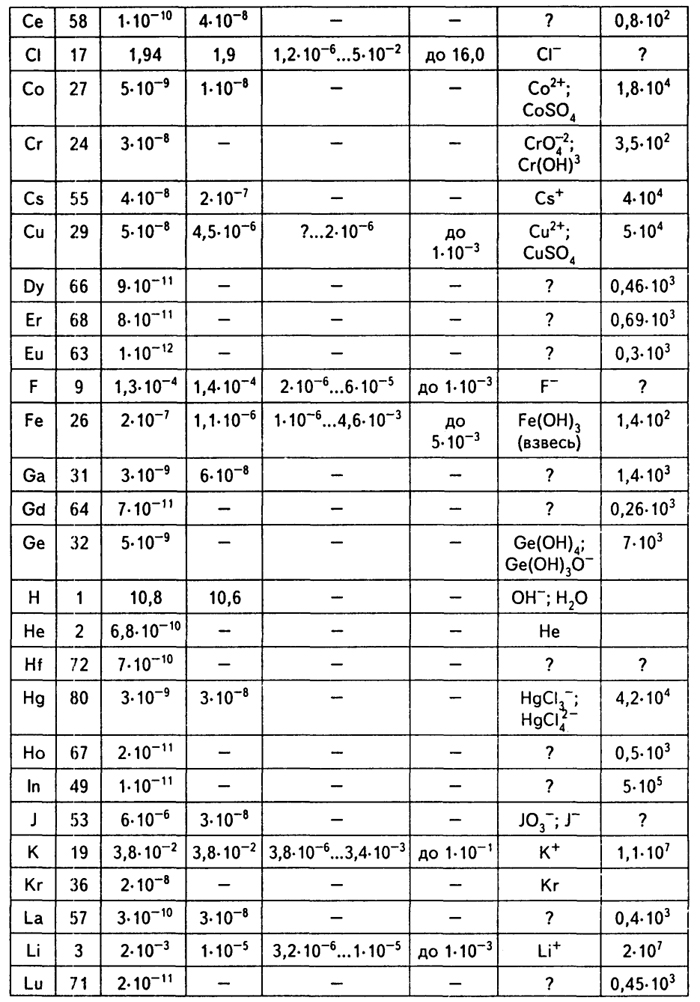
Все воды гидросферы можно разделить на две большие группы: минерализованные воды Мирового океана и преимущественно пресные воды континентов. В обеих группах установлены средние содержания (кларки) большинства химических элементов (табл. 3.5).
Геохимическая обстановка развития жизни в Океане отличалась от обстановки на континентах прежде всего наличием водной среды, содержащей большинство химических элементов в наиболее доступной для организмов форме – в ионных растворах (см. табл. 3.5). Как видно из рис. 3.3, кроме ионов в океанической воде растворены газы, а также находятся минеральные и органические коллоиды и отдельные молекулы различных веществ. Первичная минерализация вод Океана неизвестна, но вполне можно считать, что они были менее солеными. Косвенно об этом свидетельствует миграция многих видов морских рыб на нерест в пресные воды рек и озер.
Эксперименты показывают, что океаническая вода представляет собой раствор, ненасыщенный химическими элементами. Специалисты считают, что определенная концентрация в водах большинства химических элементов
57
Таблица 3.5
Кларковые содержания элементов в водах, массовые %;

58
Продолжение таблицы 3.5
59
Продолжение таблицы 3.5

60
Продолжение таблицы 3.5

поддерживается в результате механического опускания частиц, сорбции и биогенной аккумуляции. Эти три основных механизма извлечения химических элементов (их соединений) из вод тесно переплетены между собой и неодинаково проявляются в разных частях Океана. По данным академика А. П. Лисицина и ряда других исследователей, биогенное осадконакопление резко преобладает в гумидных областях. А вообще зоопланктоном за 20 суток отфильтровываются воды Океана до глубины 500 м. (Теперь вспомним, что под пленкой нефти в водах пропадает жизнь, что зоопланктон гибнет от ядохимикатов, и представим иллюзорность самоочищения Океана при современном отношении к его загрязнению.)
61

Рис. З.З. Среднее содержание химических элементов (м /л)
в морской воде (по Л. Хендерсону, с дополнениями) и основные формы
существования элементов (по данным разных авторов).
Ведущие элементы обведены жирной линией
62
Все три механизма извлечения химических элементов (их соединений) из вод не постоянны во времени и пространстве. В связи с этим в зависимости от времени, глубины водного слоя и местоположения в Мировом океане концентрация одного и того же элемента может изменяться в довольно широких пределах. Так, анализы вод показали содержание в них меди у Шотландского побережья и в Адриатическом море около 6 (в мкг/л), в Ла-Манше – 12, у восточного побережья США – 16, а в Ирландском море – 27. У ряда других элементов (особенно у поглощаемых животными организмами) пределы колебаний еще больше, а для С, N, О, Р, S и Si они достигают трех порядков (Е.D. Goldberg, 1957).
Возрастает объем взвесей, выносимых реками в Океан с освоенных людьми территорий, их значительную часть составляют коллоидные частицы. Таким образом, в результате антропогенной деятельности возможно изменение кларковых содержаний, определяющих состав вод в настоящее время. Вероятность этого увеличивается в связи с тем, что не только изменяется состав вод, поступающих с континентов, но под действием антропогенных процессов меняются природные процессы всех трех видов извлечения химических элементов из океанических вод.
Сейчас еще трудно сказать, начинаются ли в результате техногенной нагрузки на Океан процессы мутации водных организмов, однако миграция многих из них из загрязненных вод в более чистые хорошо видна на примере Черного моря. Пока наибольшие техногенные изменения элементного состава характерны для пресных вод континента. Но природные колебания содержаний отдельных элементов в поверхностных и подземных водах континентов очень велики (табл. 3.5). В связи с этим можно предполагать, что в настоящее время на жизнь организмов в этих водах большее влияние оказывают не изменения концентраций химических элементов, а появление техногенных соединений, не имеющих аналогов в этих условиях.
Отличия содержаний кларков химических элементов в водах Океана и пресных водах континентов (рек) для подавляющего большинства элементов не существенны (табл. 3.5). Если учесть еще и подземные минерализованные воды, то в водах Океана кларки элементов будут находиться между крайними значениями (минимальными и максимальными) средних концентраций этих же элементов в разных типах вод континентов (табл. 3.5).
63
Можно считать, что кларки, определенные для нынешнего состояния гидросферы, в наибольшей мере отвечают, во-первых, условиям жизни водных организмов, а во-вторых – миграции элементов, обеспечивающей нормальную жизнедеятельность современных организмов суши.
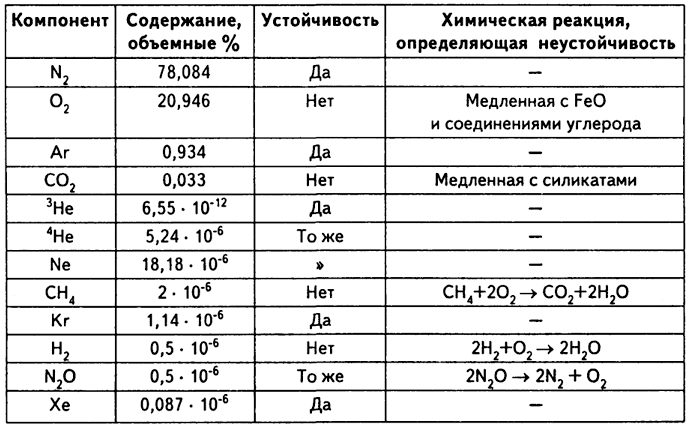
Атмосферные газы (табл. 3.6) часто рассматривают совместно с почвенными, так как они вместе определяют процессы жизнедеятельности многих организмов суши.
Кроме перечисленных в табл. 3.6 газов и паров воды, в атмосфере находятся радиоактивные газы (радон и торон), которые иногда (особенно Rn) скапливаются в приземном воздухе, даже в помещениях. Обычно это происходит над залежами урана и тория и над разрывными нарушениями в земной коре. Скопления природных радиоактивных газов могут оказать отрицательное воздействие на жизнедеятельность человека. В последнее время такие образования чаще имеют техногенное происхождение и связаны с "мирным использованием атома".
В воздухе также всегда присутствуют аэрозоли (см. табл. 3.6). Их природная концентрация над континентами измеряется десятками микрограммов
Таблица 3.6
Постоянные компоненты атмосферного воздуха
64
в 1м3 газа; над океанами она на порядок меньше. Максимальное содержание аэрозолей отмечается непосредственно над поверхностью Земли и резко уменьшается до высоты 5 км. Изучение состава аэрозолей показало, что в районах отсутствия промышленных предприятий они содержат микроэлементы в следующих концентрациях (в нг/м3*):
n·10 : Zn > Сu > Мn > Сr > Рb > V > Ni > As;
n: Cd > Se > Со; Hg ∼ 1 - 2; Sb ≈ 1; Sc ∼ 0,1 - 1,0.
Такие концентрации рассматриваемых элементов обычны и считаются безвредными.
Значительная часть живого вещества используется в качестве продукта питания для другой его части, включая человека. Основное количество химических элементов, обеспечивающих нормальные процессы жизнедеятельности, люди получают за счет потребления растительных и животных организмов. Содержание элементов в различных видах растений и животных изменяется в довольно широких пределах. Кларковое содержание рассчитано пока только для всей массы живого вещества. При этом за основу бралась фитомасса (масса растительных организмов), резко преобладающая над зоомассой. Данные о среднем содержании ряда химических элементов, наиболее распространенных в живом веществе, приведенные в табл. 3.3 (кларки живого вещества), можно рассматривать как оптимальные для всего блока живого вещества, хотя для отдельных видов (например, для человека) они могут отличаться от приведенных значений (см. табл. 3.4).
По мнению В.И. Вернадского, большая часть химических элементов, составляющих общую массу живого вещества, раз попав в него, практически в нем и остается все время, переходя из одних организмов в другие, включая человека. Однако следует отметить, что существует постоянный отток элементов из живого вещества в окружающую среду в виде газов, водных растворов и минеральных соединений. Например, при бактериальном разложении многих органических соединений образуются газы (преимущественно СО2) и вода. Часть отмерших организмов (в первую очередь скелетные образования, раковины, еще в теле живого организма состоявшие из минеральных соединений) переходит в значительной мере в косное минеральное вещество.
65
В свою очередь многие химические элементы, ранее входившие в состав косного вещества биосферы, постепенно переходят в живое вещество. К ним относятся не только О, N, Н, С, Са, Мg, но и те, которые составляют менее 0,001% их массы, в том числе металлы. Их количество в результате разнообразных процессов жизнедеятельности людей значительно возросло во всех частях биосферы. В отдельных случаях их концентрация достигла значений, нарушающих саму безопасность этой жизнедеятельности. Многие данные о поглощении металлов организмами (в первую очередь растительными) были получены в процессе поисков месторождений полезных ископаемых при помощи опробования растений (биогеохимическими методами).
Оказалось, что при аномально высокой концентрации отдельных элементов в среде, окружающей и питающей организмы, последние в своем подавляющем большинстве не могут противостоять вхождению в них этих элементов. При этом существенно повышенная концентрация в организмах одних элементов может вызвать повышение или же понижение концентраций в этих же организмах других элементов, независимо от концентрации последних в окружающей среде (В.А. Алексеенко, 1969). Иными словами, аномально высокое содержание в окружающей среде даже одного химического элемента может привести к дисбалансу многих элементов в организме. Аналогично действует на организмы и недостаточная концентрация каких-либо химических элементов в окружающей среде.
Таким образом, и избыток, и недостаток химических элементов в окружающей среде отрицательно сказываются на состоянии живых организмов, а при определенных дозах могут вызвать их смерть. Люди это знали очень давно и не просто использовали целый ряд химических элементов (и их соединений) в качестве ядов, а пытались обезопасить свою жизнь нормированием их концентраций в среде, из которой они могут попасть в организм. До нас дошли сведения о том, что еще в средние века в Германии были сделаны первые попытки государственного нормирования поступления свинца – тяжелого металла, расположенного много ниже "линии жизни", в человеческий организм. В 1548 и 1577 гг. в этой стране были приняты законы, по которым подмешивание свинца к вину (а это делалось для подслащения и улучшения вкусовых качеств) каралось смертной казнью. Позже там же был принят закон, по которому в оловянной посуде ограничивалось содержание свинца.
66
Довольно давно люди стали и восполнять недостаток определенных химических элементов, поступающих в их организм, для лечения болезней, вызываемых этим недостатком. При расстройстве нервной системы врачи издавна "прописывали бром" (точнее небольшие дозы солей брома). Во избежание порчи зубов, вызванной недостатком фтора, фторируют зубную пасту и питьевую воду. Например, в Пуэрто-Рико эти мероприятия на 65% уменьшили развитие кариеса зубов у детей. (Однако избыток F приводит к разрушению зубной эмали.) Государственный масштаб принимает иодирование пищевой соли (NaCI). Это позволяет избежать ряда болезней, включая такую страшную, как кретинизм. Во всех перечисленных случаях используются только легкорастворимые, а следовательно, и хорошо доступные человеку соединения рассмотренных элементов.
Таким образом, чрезвычайно важно учитывать формы нахождения химических элементов как в среде обитания, так и непосредственно в продуктах питания организмов (включая человека). Формами нахождения химических элементов в среде обитания и в продуктах питания организмов во многом определяются:
- состав живого вещества, соотношение в нем химических элементов;
- доступность элементов живым организмам (включая человека) и скорость поступления элементов в организмы;
- постепенное влияние на организмы изменения концентрации в окружающей среде элементов, даже находящихся в довольно устойчивой в условиях биосферы минеральной форме, о чем можно судить по смене растительных ассоциаций при изменении почвоподстилающих (почвообразую-щих) пород. Передаваясь по трофическим цепям, такие изменения могут воздействовать на здоровье человека. При этом в определенных случаях может уменьшаться безопасность жизнедеятельности.
Распределение химических элементов в среде обитания организмов. Проблема установления границ безвредных концентраций химических элементов в окружающей и питающей среде довольно давно стояла перед человечеством. Развитие и существование жизни на Земле, кроме двух рассмотренных факторов (содержание и форма нахождения химических элементов в среде обитания), обусловлены еще и распределением элементов в той крупной геохимической системе, которая является окружающей (питающей) средой для рассматриваемых организмов. Если говорить о жизни на Земле вообще
67
(а сюда входит и жизнь людей), то геохимической системой, составляющей окружающую среду для всего блока живых организмов, будут верхние части земной коры. Рассмотрим распределение химических элементов в верхних частях земной коры и его изменение во времени. Для этого были введены такие понятия, как абсолютный и относительный разброс, характеризующие сложные неоднородные геохимические системы (В.А. Алексеенко, 1997).
Абсолютный разброс (АР) представляет собой отношение максимального фонового содержания элемента в одной части неоднородной геохимической системы к минимальному фоновому в другой части этой системы. В случае земной коры частями этой неоднородной геохимической системы являются участки, сложенные породами разных типов. Вместо фоновых содержаний при изучении рассматриваемой системы нужно использовать кларковые содержания пород различных типов.
Относительный разброс (ОР) представляет собой отношение значений абсолютных разбросов одного и того же элемента в рассматриваемой геохимической системе до и после изучаемых процессов. Можно считать, что в первый период существования планеты Земля ее поверхность была сложена магматическими породами. Следовательно в этот период АР каждого элемента характеризовался отношением его кларкового содержания в одном типе магматических пород к минимальному в другом типе магматических пород (см. табл. 3.2). Полагая, вслед за В.И. Вернадским, что жизнь на Земле возникла практически одновременно с ее формированием, можно считать, что в этот период значения АР в магматических породах определяли оптимальные колебания содержаний элементов в среде обитания всего блока живых организмов.
Как видно из табл. 3.2, значения АР для разных элементов рассматриваемого периода существования Земли колебались от 1,3 до 127. Чем меньше были значения АР отдельных элементов, тем к меньшим последующим изменениям содержаний этих элементов были "подготовлены" первые организмы.
В процессе своего развития и жизнедеятельности эти организмы способствовали выветриванию магматических и образованию за их счет осадочных пород. В результате в геохимической системе, представляющей поверхность Земли (в горных породах континентов), изменились значения АР (табл. 3.2). Мерой этих изменений стал ОР. В этот период элементы с большими значениями
68
ОР должны были сильнее воздействовать на развитие жизни и появление мутантов. Такими элементами на континентах можно считать (с учетом их положения относительно линии жизни) Hg, S, Se, N, В (В.А. Алексеенко, 1997).
Дальнейшие изменения АР, охватывающие значительные части поверхности Земли, были связаны с космическими катастрофами и с формированием региональных геохимических аномалий рудных районов и узлов. К настоящему времени значение АР<10 характерно лишь для Bi, W, Аu, Вr, Р, Zn, Ag, J, Be (табл. 3.2). Если за граничное значение принять 20, то к перечисленным элементам добавятся As, Cd, Ga, Mo, Pb, S, V, Yb, Sn, F, и ряд лантаноидов. Резкое увеличение их разброса в результате техногенных процессов может вызвать крайне нежелательное воздействие на развитие жизни вообще и на безопасность жизнедеятельности людей.
Антропогенные процессы, приводящие к загрязнению среды, окружающей человека, способствуют глобальному усилению неравномерности распределения химических элементов и возрастанию АР. В этом направлении наибольшие изменения могут в первую очередь произойти в распределении вышеперечисленных химических элементов с малыми значениями АР.
Анализируя сказанное о распределении во времени химических элементов на поверхности Земли, можно считать, что:
- изменяющееся распределение элементов не могло не повлиять на развитие организмов;
- основные изменения АР, связанные с появлением и площадным развитием донных океанических осадков и осадочных пород, происходили постепенно, эволюционно. Кроме них были и изменения АР, развивающиеся катастрофически быстро. Они оказывали наибольшее негативное воздействие на существовавшие в то время организмы, что и подтверждается имеющимися данными;
- последствия современных антропогенных процессов по своей значимости и скорости развития приближаются к катастрофическим изменениям АР в истории Земли. Это необходимо учитывать при решении вопросов, связанных с проблемами безопасности жизнедеятельности.
Подводя итог рассмотрению влияния химического состава среды обитания организмов на развитие этих организмов, можно сделать следующие выводы:
69
- Наиболее опасными для развития живых организмов, а следовательно и для всех процессов жизнедеятельности людей являются последствия антропогенной деятельности, приводящие к увеличению неравномерности распределения химических элементов и к значительному возрастанию ОР по отношению к АР в породах и почвах континентов.
- Необходимо учитывать, что районы с повышенным содержанием элементов, расположенных в удалении и ниже линии жизни, менее благоприятны для жизнедеятельности людей.
- Среди районов с существенно пониженной концентрацией отдельных химических элементов менее благоприятны те, в которых понижены концентрации элементов, находящихся на линии жизни или вблизи нее.
- Среди рассмотренных химических элементов для человека наиболее опасны резко повышенные и резко пониженные концентрации тех из них, которые находятся в форме различных водных растворов, аэрозолей, хорошо растворимых соединений и биогенных соединений, представляющих собой продукты питания.
- Ориентировочно "безвредными" для жизнедеятельности человека, как и подавляющего большинства живых организмов, могут считаться кларковые содержания химических элементов в горных породах и почвах, в пресных и морских водах, в атмосферном воздухе и в живом веществе, представляющем собой продукты питания. Именно в районах с содержаниями элементов, близкими к кларковым, безопасность жизнедеятельности с точки зрения геохимических особенностей среды обитания людей может считаться наибольшей.
70
