Цепные реакции отличаются от обычных тем, что при их протекании элементарные акты не независимы друг от друга, каждый происшедший акт вызывает один или несколько других. Это обусловлено тем, что возникающие в результате реакции частицы обладают повышенной химической активностью.
Цепные реакции представляют собой обширный класс процессов, имеющих большое практическое значение (горение, крекинг нефти, производство пластических масс - полимеров, атомная энергетика).
Ведущая роль в развитии теории цепных реакций и открытии новых факторов в этой области принадлежат акад. Н.Н. Семенову и возглавляемой им советской научной школе. Важный вклад в теорию цепных реакций внесли М. Боденштейн, В. Нернст и особенно Ч. Гиншельвуд.
Цепные реакции были открыты при изучении фотохимических процессов. Еще в прошлом веке было известно, что если смесь хлора и водорода подвергнуть интенсивному освещению, то происходит быстрая реакция образования HCl, которая при известных условиях может приобрести характер взрыва.
В начале XIX в. Ф.И. Гротгус открыл закон, гласящий, что фотохимические реакции могут вызываться лишь теми световыми лучами, которые поглощаются реагирующими веществами. В 1905 г. А. Эйнштейном был установлен закон фотохимической эквивалентности, согласно которому каждая
453
молекула, реагирующая, под влиянием света, поглощает только один квант излучения, вызывающий реакцию. Поэтому система, в которой прореагировало N молекул, должна поглотить энергию Е в соответствии с уравнением
E = Nhν = Nh
,
(XVII.1)
где ν - частота излучения; с - скорость света; λ - длина волн света.
Обычно число прореагирующих молекул не равно числу поглощенных квантов. Отношение числа фактически прореагировавших молекул к числу поглощенных квантов (E/hν) называется квантовым выходом. Эта величина бывает меньше, больше и равна единице. Например, при диссоциации аммиака
NH3г = 1/2N2г + 3/2H2г
квантовый выход близок к 0,75. Это означает, что число поглощенных квантов больше числа распадов, т.е. часть поглощенной лучистой энергии превращается в тепловую. При диссоциации H2S под воздействием света с длиной волны 208 нм квантовый выход равен единице.
Первичной реакцией при образовании озона, происходящей в результате облучения кислорода ультрафиолетовым светом, является диссоциация:
О2 + hν = О + О
с последующими реакциями атомарного кислорода: O + O2 = O3; O + O2 = O3.
Таким образом, один квант вызывает превращение трех молекул кислорода.
В упоминавшейся выше реакции образования HCl квантовый выход очень велик и составляет величину порядка 105. В связи с этим М. Боденштейн предложил цепной механизм подобных реакций, при котором фотохимическая реакция только начинает цепь и не играет никакой роли в дальнейшем протекании цепной реакции. Эта мысль подтверждается наблюдениями, согласно которым реакция Н2г + Сl2г = 2HClг начинается лишь через некоторое короткое время после освещения смеси и продолжается после его прекращения. В течение начального периода увеличивается концентрация свободных атомов и, следовательно, скорость реакции. Для рассматриваемой реакции В. Нернст предложил следующий механизм:
454
С12 + hν = 2С1; Cl + Н2 = HCl Н + Н;
Н + С12 = HCl + Cl и т.д.
Другими примерами цепной реакции являются процессы
CH4 + Cl = CH3 + HCl и CH3 + Cl2 = CH3Cl + Cl.
Таким образом, во всякой цепной реакции процесс развивается вследствие образования неустойчивых промежуточных продуктов - атомов или радикалов, которые называются также активными центрами. Важно подчеркнуть, что эти промежуточные вещества являются валентно ненасыщенными. Вследствие неустойчивости атомов и радикалов время их жизни очень мало.
Возникающие при проявлении атомов или радикалов цепи либо неограниченно развиваются, что приводит к взрыву, либо обрываются вследствие гибели активных центров в результате адсорбции на стенках сосуда или тройных соударений в объеме смеси.
Таким образом, для цепных реакций характерны три следующие стадии: 1) зарождение (первичная реакция); 2) развитие; 3) обрыв.
Зарождение цепи происходит не только под влиянием света, но и под воздействием излучений радиоактивных веществ, а также благодаря введению в систему свободных атомов. Например, если в смесь H2 и Cl2 ввести пары натрия, то образующиеся при реакции Na + Cl2 = NaCl + Cl атомы хлора являются причиной возникновения хлорводородных цепей.
В некоторых случаях начало цепных реакций обусловлено добавлением к реакционной смеси веществ, атомы которых поглощают свет определенной длины волны и становятся активными. Так, при облучении паров ртути возбужденные атомы Hg* при соударениях с молекулами реагирующих веществ вызывают их распад и, следовательно, образование цепей, например,
Hg* + Н2 = HgH + Н.
Возникновение цепей может происходить вследствие самого акта химической реакции, при которой образуются радикалы. Кроме того, образование атомов или радикалов может быть вызвано высокой температурой реакционной смеси или наличием катализаторов.
Интересной иллюстрацией этого может служить реакция образования Н2О. Если при низких давлениях и температуре ∼5300С направить перпендикулярно друг другу
455
потоки водорода и кислорода таким образом, чтобы они встретились в центре большого сосуда, то реакция не начнется. Однако, если эти газы смешать в малом сосуде из кварца или фарфора, то реакция сопровождается взрывом. Введение кварцевой трубки в центр большого сосуда также приводит к развитию реакции при смешении водорода и кислорода. Предполагалось, что это объясняется образованием на поверхности кварца гидроксильных радикалов: Н2 + О2 = 2ОН, которые приводят к образованию цепей.
Цепная реакция соединения водорода с кислородом может быть вызвана и внесением в смесь губчатой платины на поверхности которой происходит диссоциация Н2 на атомы. Реакция окисления СО кислородом, имеющая взрывной характер, вовсе не происходит при полном отсутствии водяных паров. Это объясняется трудностью разрыва прочной связи в молекулах О2. В присутствии же влаги эта реакция развивается как цепная.
Из сказанного следует, что первая стадия цепных реакций может быть вызвана самыми различными способами.
Рассмотрим вторую стадию цепных реакций - развитие цепей. При этом будем различать реакции с простыми и разветвляющимися цепями. В первом случае каждый исчезающий атом или радикал вызывает появление лишь одного нового атома или радикала. Примером такой неразветвленной цепи может служить упоминавшаяся выше реакция между Н2 и С12.
В реакциях с разветвляющимися цепями на каждый исчезающий центр реакции возникает несколько новых. К числу таких реакций, в частности, принадлежит уже рассматривавшийся процесс окисления водорода. При низких давлениях и температуре около 500° C он может развиваться согласно следующей схеме:
Н + O2 = ОН + O;
ОН + Н2 = Н2O + Н;
О + Н2 = ОН + Н и т.д.
Существование свободных атомов и радикалов было доказано различными методами. Так, в реакционную смесь вводят специальные зонды, снабженные чувствительными малоинерционными термопарами, покрытыми катализаторами. На поверхности таких катализаторов происходят процессы рекомбинации атомов и радикалов, сопровождающиеся значительным выделением тепла. Например, катализатор ZnO·Cr2O3 ускоряет реакцию рекомбинации атомов
456
водорода. По повышению температуры зонда можно определить концентрацию свободных частиц. Спектроскопическим путем определяют концентрацию радикалов ОН (В.Н. Кондратьев). В последнее время возникающие при цепных реакциях радикалы исследуются методом электронного парамагнитного резонанса (см. гл. XXIV).
Наличие свободных органических радикалов при реакции в газовой фазе было доказано работами Ф. Пакета, который пропускал через кварцевую трубку пары тетраэтил-свинца (С2Н5)4Рb в быстром токе водорода. При нагревании участка трубки на ее стенке выделился металлический свинец и образовались свободные радикалы C2H5. Если на небольшом расстоянии от этого места по течению газовой смеси таким способом был заранее нанесен свинец, то под действием радикалов он вновь давал тетраэтилсвинец и удалялся с внутренней стенки трубки. Зная скорость газового потока и наблюдая за появлением и удалением налета свинца, удалось вычислить, что период, в течение которого концентрация свободных радикалов этила падает в два раза, составляет 3·10-3 с.
Образование свободных радикалов при термической диссоциации (С2Н5)4Рb связывалось с влиянием этого вещества как антидетонатора при горении бензина в двигателях внутреннего сгорания.
Последняя, третья, стадия цепных реакций представляет собой процесс гибели активных частиц (атомов и радикалов).
Как уже отмечалось, двойные столкновения атомов или радикалов не приводят к реакции вследствие трудности отвода энергии, а приводят к акту реакции лишь при тройных столкновениях с участием молекул реагентов или примесей М, например, СО + О + М = M* - СО2.
Часто обрыв цепей происходит на стенках сосуда вследствие адсорбции Н → Надс.
Явление обрыва цепей было продемонстрировано в сыгравших решающую роль в развитии учения о цепных реакциях опытах Н.Н. Семенова, показавшего, что добавление инертного газа (Ar) оказывает влияние на ход реакции между парами фосфора (P4) и кислородом. При низких давлениях цепи обрываются из-за взаимодействия активных центров - атомов кислорода со стенками сосуда. Повышение давления аргона затрудняет диффузию атомов кислорода к стенкам сосуда. Вследствие этого в объеме происходит цепная реакция окисления, развитие которой сопровождается так называемым холодным пламенем.
457
Интересный механизм обрыва цепей наблюдается при некоторых реакциях окисления. Он обусловлен образованием неустойчивого соединения НО2, соответствующего тетраокисям щелочных металлов (NaO2, KO2). Присутствие этого соединения в реакционных смесях было доказано спектроскопическими методами. Возникновение и гибель атомов и радикалов вследствие образования НО2 может происходить следующим путем:
Н + О2 + М = НО2 + М;
НО2 = ½Н2 + О2 (на стенках сосуда), где М - молекула примеси.
Влияние примесей на протекание многих реакций, которое было известно уже давно, получило объяснение с точки зрения теории цепных реакций. Особую роль в протекании широкого круга процессов в качестве примеси играет вода. Так, было показано, что при тщательной осушке Р, Na и К не соединяются с кислородом, а смесь Н2 и Cl2 не реагирует на свету. Оказалось, что для протекания последней реакции достаточна концентрация воды, составляющая 10-5 %. Таким образом, вода является катализатором для ряда реакций.
Вещества, добавление которых приводит к сокращению длины цепей, называются ингибиторами. Например, присутствие следов кислорода в смеси водорода и хлора препятствует протеканию реакции образования HCl. Это объясняется тем, что ингибиторы соединяются со свободными частицами. В данном случае кислород дает с атомами водорода радикалы НО2, которые легко дезактивируются на стенках сосуда.
При изучении реакции окисления паров фосфора Н.Н. Семеновым в Ч. Гиншельвудом было открыто совершенно новое явление, характерное только для цепных реакций. Оно состоит в том, что для таких реакций существуют так называемые нижний и верхний пределы воспламенения (взрыва). Другими слонами, в некоторой области давлений процесс носит взрывной характер, а при малых и больших давлениях процесс развивается стационарно, т.е. с конечной постоянной скоростью.
При низких давлениях активные центры (например, атомы кислорода) сравнительно часто достигают стенок сосуда и дезактивируются. Очевидно, это происходит тем чаще, чем больше отношение поверхности стенок сосуда к его объему. Обрыв цепей на стенках сосуда при низких давлениях не компенсируется актами разветвления цепей, и скорость реакции конечна и мала. Увеличение давления реагирующего или инертного газа или изменение формы сосуда с уменьшением отношения поверхности его стенок к объему затрудняют обрыв цепей.
При некотором критическом давлении число гибнущих атомов или радикалов в единицу времени станет меньше, чем число вновь возникших атомов или радикалов, и скорость реакции начнет быстро возрастать, вследствие чего произойдет воспламенение смеси. Нижний предел воспламенения сравнительно слабо зависит от температуры. Наличие верхнего предела обусловлено увеличением скорости обрыва цепей в результате столкновений активных частиц с молекулами газа в объеме сосуда по сравнению со скоростью разветвления цепей. Так, в случае окисления фосфора повышение давления кислорода примерно до 1 ат приводит к прекращению горения. Если же откачать часть кислорода, то фосфор вновь загорается. Верхний предел воспламенения мало зависит от формы сосуда, но сильно зависит от температуры и наличия примесей.
458
Следует различать взрывы цепного характера, обусловленные бесконечным увеличением числа активных центров, и тепловые взрывы. Тепловые взрывы происходят вследствие того, что при экзотермических реакциях не успевает отводиться тепло. С повышением температуры ускоряется протекание реакции. В результате происходит неограниченное возрастание скорости реакции. Изображенная на рис. XVII.1 кривая схематически показывает предельные условия, при которых происходят взрывы.
Штриховкой на этом рисунке обозначена область взрывов. При температуре T1 точка а указывает нижний предел взрыва, а точка б - верхний. Выше точки б может начаться при давлении, большем в только тепловой взрыв.
А.Г. Мержанов открыл новый тип твердофазных реакций, в которых происходит горение без участия кислорора. Они распространяются подобно взрывам.
В качестве горючего в подобных реакциях участвуют такие металлы, как Ti, Zr, Hf, Nb, Та и др., а окислителями являются неметаллы В, С, Si, N. Особенность таких процессов заключается в том, что они сопровождаются очень большим выделением тепла. Большое выделение тепла наблюдается и при реакциях переходных металлов с благородными металлами. Например, в смеси порошков гафния и платины или циркония и платины при тепловом инициировании происходит взрыв с образованием соединений Pt3Hf и Pt3Zr. При образовании моля Ni3Si выделяется около 150 кДж тепла. При подобных экзотермических реакциях тепло не успевает рассеиваться, и они протекают в режиме, близком к адиабатическому. В результате в объеме реагирующей смеси развивается очень высокая температура (до 4000° C). Это в свою очередь приводит к дальнейшему распространению зоны реакции по механизму, напоминающему взрывные процессы в газовых смесях. Такой характер горения используют в технике для синтеза многих соединений металлов, особенно тугоплавких. С этой целью приготавливают смеси реагирующих веществ в виде порошков и инициируют реакций) либо нагреванием электрической
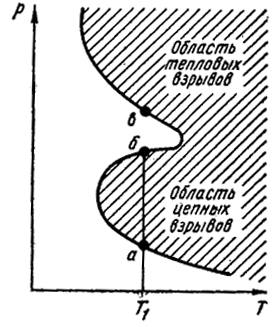
Рис. XVII.1. Граница областей взрывов
459
спирали, либо при помощи химического запала. Дальнейшее развитие процесса сопровождается ярким свечением, которое указывает на быстрое, волнообразное движение фронта горения. Этот метод получил название самораспространяющегося высокотемпературного синтеза (СВС). "При помощи СВС в течение секунд происходит полное превращение смеси исходных веществ в монолитный продукт реакции, в ряде случаев даже в виде готового изделия с определенной формой. Метод СВС используют для производства не только тугоплавких, но и жаростойких, износостойких материалов с высокой твердостью, материалов с большим сопротивлением воздействию агрессивных сред. Такие материалы обычно представляют собой композиции на основе боридов, силицидов, нитридов, оксидов и карбидов переходных металлов.
Важную разновидность цепных реакций представляют процессы полимеризации, при помощи которых в настоящее время производятся многочисленные синтетические материалы. Процессы полимеризации отличаются от обычных цепных реакций тем, что при их протекании возникающие радикалы не регенерируются, а образуют радикалы с более высокой молекулярной массой, что происходит благодаря соединению их с мономерами. Процессы полимеризации инициируются добавлением веществ, легко отщепляющих радикалы (обычно органические перекиси). Примером такой реакции может служить полимеризация винилхлорида СН2 = СHCl, в которой цепи возникают в результате расщепления перекиси бензоила:
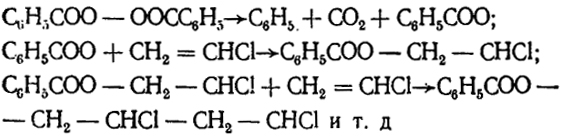
Здесь две параллельные черты указывают на двойные связи между атомами углерода.
Свойства синтетического каучука в значительной степени зависят от длины составляющих его молекулярных цепей. Для регулирования длины цепей в смесь добавляют какое-либо вещество, легко отдающее атом водорода (например, меркаптан) свободному радикалу, находящемуся на конце растущей молекулы каучука. Таким образом, эта цепь обрывается и возникает новый радикал, являющийся инициатором роста другой молекулы каучука. Вследствие этого регулятор разрывает молекулы каучука на цепи определенной
460
длины, не прерывая развития процесса полимеризации. Примером веществ-регуляторов являются витамины E и С, которые обрывают цепные окислительные реакции в организме человека.
Изложенное выше показывает, что отличительными чертами цепных реакций являются следующие:
- 1) большой квантовый выход при фотохимическом возбуждении;
- 2) высокая чувствительность к присутствию примесей;
- 3) зависимость скорости от формы и размера сосудов, в которых протекают реакции;
- 4) наличие верхнего и нижнего пределов воспламенения.
Цепные реакции могут протекать с очень малыми и большими скоростями.
461
