Основной особенностью адсорбции на поверхностях раздела жидких фаз является возможность измерения поверхностного натяжения. Надежных методов измерения поверхностного натяжения твердых тел нет, так как обратимое изменение их поверхности встречает ряд трудностей.
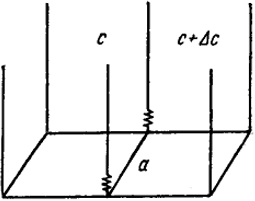
Рис. XV.8. Схема к выводу уравнения Гиббса
Между поверхностным натяжением и адсорбцией есть связь, описываемая уравнением Гиббса, являющимся одной из основ всей области поверхностных явлений.
Чтобы понять физический смысл этой связи, рассмотрим сначала следующий простой случай. Пусть над жидкой поверхностью имеются два отделения (рис. XV.8), в которых находится некоторое газообразное вещество, практически не растворимое в жидкости. В левом сосуде оно имеет концентрацию с, а в правом с + Δс.
На рис. XV.8 показано, что, двигая по поверхности пленку, можно менять поверхность жидкости над каждым отделением. Передвинем пленку вправо так, чтобы 1 см2 этой поверхности перешел в левое отделение из правого. Тогда слева произойдет адсорбция газа на вновь образующейся поверхности и Г молей исчезнет из левого отделения. В правом отделении произойдет десорбция молей. При этом Г молей будут переведены от концентрации с до концентрации с + Δс. Это требует затраты работы:
407
ГRTln[(c + Δc)/c] = ГRTln[1 + (Δc/c)] = ГRT(Δc/c).
В целом система работает как насос, увеличивая обратимо и изотермически с. Необходимая для этого работа, равная Δσ, получается при передвижении пленки. Таким образом,
Δσ = -ГRT(Δc/c) и Г = -(c/RT)(dσ/dc).
(XV.28)
Этот вывод относится к частному случаю (двухкомпонентная система, идеальный газ и др.).
Общее рассмотрение было дано Гиббсом.
Введенное им уравнение является аналогом уравнения Гиббса-Дюгема (XV.8).
Рассмотрим систему из двух фаз.
Тогда U = U1 + U2 + Uπ, где U1 и U2 - внутренние энергии фаз; Uπ - поверхностное сгущение внутренней энергии.
Тогда
dU1 = TdS1 - pdV1 + ∑μidni.
При рассмотрении изменения поверхностного сгущения энергии следует учесть, что изменение площади поверхности раздела потребует затраты работы σdF.
Поверхностное сгущение объема равно нулю, так как, согласно определению, линия раздела проводится без изменения объема системы. Поэтому
dUπ = TdSπ + ∑μidn
+ σdF.
(XV.29)
Как и при выводе уравнения Гиббса-Дюгема, проинтегрируем это уравнение при сохранении состава фаз и постоянства Sπ, μi и σ. Тогда Uπ = TSπ + ∑μin
+ σ
F.
После дифференцирования этого уравнения при произвольном изменении числа молей получаем:
dUπ = TdSπ + SπdT +
μidni +
n
μi + σdF + Fdσ.
(XV.30)
Вычтем уравнение (XV.29) из уравнения (XV.30), тогда
Fdσ + SπdT + ∑n
dμ
i = 0.
Так как n
/
F = Г
1, а
n
/
F = Г
2 то при постоянной температуре для двухкомпонентной системы dσ = -Г
1dμ
1 - Г
2μ
2.
Выбор поверхности раздела, как указывалось, произволен. Гиббс предложил выбирать ее так, чтобы адсорбция одного компонента равнялась нулю. Пусть Г1 = 0, тогда dσ = -Г2dμ2.
408
Так как при постоянной температуре dμ2 = RTd ln a2, то
Г2 = -(a2/RT)(dσ/da2).
(XV.31)
где ai - активность компонента .
Для разбавленного раствора Г2 = (c2/RT)(dσ/dc2) и уравнение (XV.31) переходит в уравнение (XV.28).
Уравнения (XV.28) и (XV.31) являются основой для определения величины адсорбции по измерению поверхностного натяжения. Измерение σ = f(c) позволяет определить величину da/dc и рассчитать Г.
Такой метод представляет большую ценность, так как при малых поверхностях, которые обычно реализуются в системе жидкость-газ, изменение концентрации в результате адсорбции мало и применение методов, подобных описанным, для системы твердое тело-газ затруднительно.
Однако и для системы твердое тело-газ чисто возникают задачи определения адсорбции при малых поверхностях раздела, так как достаточное диспергирование не всегда возможно. Это относится, в частности, к границе твердый сплав-газ. Между тем сведения о поверхностных слоях весьма важны, так как они определяют многие прочностные и другие характеристики твердых тел.
В последнее время разработан ряд эффективных методов определения состава поверхностных слоев, позволяющих рассчитать адсорбцию.
Эти методы основаны или на зондировании поверхности металла различного типа частицами (электроны, ионы и др.), или на других способах воздействия на него (нагревание, электрическое или магнитное поле, звуковые поверхностные волны и др.). Изучается природа, распределение в пространстве и по энергии эмитируемых частиц.
В результате получается информация об элементном составе поверхностного слоя (1-10 атомных слоев под поверхностным монослоем), количестве адсорбированных на поверхности частиц и их природе.
Особенно успешно применение Оже-спектроскопии. При этом на металл направляются электроны (с энергией от 1000 до 3000 эВ). Эти электроны выбивают электроны внутренних оболочек атома. На это освободившееся место переходит другой электрон атома. Выделяющийся при этом фотон способен вызвать выделение другого электрона атома, так называемого Оже-электрона. Изучение распределения по энергиям этих электронов позволяет определить химическую природу атомов, их количество и даже природу межатомных связей.
409
Из уравнения (ХХ.33) следует, что если добавка к раствору компонента приводит к повышению поверхностного натяжения раствора (dσ/dc > 0), то его адсорбция отрицательна (Г < 0). Положительная адсорбция имеет место для веществ, понижающих поверхностное натяжение. Эти обстоятельства связаны с тенденцией раствора понизить свою поверхностную свободную энергию.
Так как поверхность F задана условиями опыта (формой сосуда, полем тяжести и пр.), то раствор стремится уменьшить величину а. Если вещество понижает поверхностное натяжение, то его излишек на поверхности будет приводить к снижению поверхностного натяжения. Вещество, повышающее поверхностное натяжение, будет удаляться с поверхности для ослабления эффекта повышения поверхностного натяжения.
Часто вещества, увеличивающие поверхностное натяжение растворителя, сами в чистом виде обладают более высоким значением поверхностного натяжения, а уменьшающие более низким по сравнению с растворителем. Большое поверхностное натяжение означает большую энергетическую насыщенность молекул, находящихся на поверхности. Такие молекулы будут удаляться с поверхности раствора, на которой для снижения свободной поверхностной энергии выгоднее иметь молекулы с малой энергетической насыщенностью. Конечно, полному разделению молекул будет препятствовать потеря энтропии образования раствора. В результате действия этих двух факторов на поверхности раствора возникает определенная адсорбция, т.е. изменение состава по сравнению с объемом. Стремление покинуть раствор и выйти на поверхность определяется условиями, которые создаются для молекул в объеме и на поверхности.
Известно, что углеводороды плохо растворимы в воде. Если органическая молекула, кроме углеводородного радикала ("хвоста"), имеет группу, имеющую сродство к воде (например, ОН, СОООН и др.), то растворимость резко возрастает.
На поверхности раздела раствора для такой молекулы осуществляется весьма выгодная в энергетическом отношении возможность. Активная группа может быть погружена в воду, а органический "хвост" убран из воды и обращен к поверхности, поэтому такие молекулы сильно адсорбируются на поверхности, резко снижая ее поверхностное натяжение. Положительно адсорбирующиеся вещества называют капиллярно-активными.
410
Примером веществ, отрицательно адсорбирующихся на поверхности воды, являются неорганические соли. Ионы стремятся уйти с поверхности, где их сильное электрическое поле не насыщено, в раствор, где может быть выиграна энергия гидратации.
На рис. XV.9 изображено изменение поверхностного натяжения стали при 1550° C в зависимости от содержания
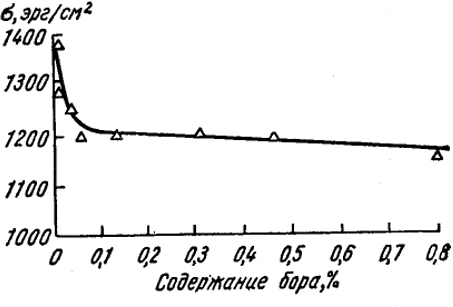
Рис. XV.9. Зависимость поверхностного натяжения жидкой стали от содержания бора
бора. Мы видим, что бор является капиллярно-активным веществом. Это обстоятельство подтверждает упомянутое выше адсорбционное толкование явления модифицирования.
411
