При рассмотрении различных систем и процессов до сих пор мы не обращали внимание на существование поверхностей раздела фаз. Так, мы полагали, что задание концентраций какого-либо-компонента во всех фазах определяет число молей этого компонента во всей системе, т.е.
ni =
Ljxi,
(XV.1)
378
где j - индекс фазы; Lj - число молей; xij - молярная доля i-того компонента в фазе.
При подсчете энергии Гиббса или любого другого интенсивного свойства системы при игнорировании границ раздела также ограничивались суммированием по фазам G = ∑Gj, где G - энергия Гиббса системы; Gj - энергия Гиббса j-той фазы.
Однако свойства фазы вблизи поверхностей раздела обличаются от свойств в середине. На поверхности может происходить специфическое поглощение компонента (адсорбция). Энергия молекул на поверхности отличается от энергии молекул в середине фаз, так как координационное число на границе меньше, чем в середине; характер движения молекул и характеристика этого движения (например, частота колебания) также будут иными на поверхности.
Возникает вопрос о целесообразных общих путях описания термодинамических свойств систем с учетом поверхностей раздела. Г. Гиббс для этой цели ввел понятие поверхностного сгущения свойств. Для учета того, что вносят в величину свойства поверхности раздела, необходимо ввести суммирование не только по объемам фаз, но и на поверхностям их разделов1:
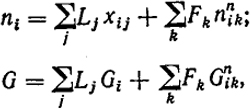
где n
- поверхностное сгущение
i-того компонента на
k-той границе раздела;
G
- сгущение энергии Гиббса на этой границе.
Эти величины характеризуют вклад, который дополнительно вносит каждая поверхность раздела в величину свойств. Если увеличить какую-либо поверхность раздела при сохранении без изменения всех остальных поверхностей разделов, объемов фаз и концентрации компонентов, то число молекул в системе (или величина любого свойства) изменится. Получится поверхностное сгущение, если отнести это изменение к единице поверхности раздела. Таким образом, поверхностное сгущение энергии Гиббса G характеризует увеличение ее при увеличении поверхности
379
раздела на единицу поверхности. Если температура и давление заданы, то, как было показано в гл. II, это изменение описывает работу, которую надо совершить для осуществления процесса.
В случае однокомпонентной системы работа обратимого увеличения поверхности определяет поверхностное натяжение (σk). Случай растворов будет рассмотрен ниже.
Поверхностное сгущение i-того компонента на k-той границе раздела называют адсорбцией на этой границе и обозначают Гik:
n
= Г
ik.
Понятие поверхностного сгущения содержит неопределенность, связанную с выбором поверхности раздела, по обеим сторонам которой мы считаем концентрации в объемах постоянными.
Мы остановимся ниже на рациональном способе выбора такой поверхности раздела.
Наряду с адсорбцией возможно поглощение в объеме тела - "абсорбция". Оба явления объединяются словом "сорбция".
Величина Гik может быть положительной (если молекулы компонента притягиваются к поверхности) и отрицательной (молекулы отталкиваются от нее).
Можно рассматривать поверхностное сгущение энтропии S
, внутренней энергии
U
и других функций.
380
1
В этой главе, чтобы отличить обозначения энтропии и поверхности для последней, введена буква
F.
