Вычисленные статистическими методами термодинамические функции могут быть использованы для расчета химического равновесия по формулам гл. III.
Однако представляет интерес, непосредственный расчет константы равновесия по спектроскопическим данным.
Рассмотрим реакцию A + 2B = D.
Условие равновесия
-GA - 2GB + GD = 0
или, учитывая формулу (XIII.3):.
RTln
+ 2
RTln
-
RTln
= 0,
или
ZDN
/ZAZ
= 1.
(XIII.12)
Здесь Z содержит объем в качестве множителя. Поэтому положим
Zi = PiVi,
где Pi носит название функции распределения.
Исключив Z из уравнения (XIII.12) и учитывая, что концентрация ci равна
, получим
cD/cAc2B = PD/PAP2B
Таким образом:
Kc = PD/PAP2B.
(ХIII.13)
При расчете функций распределения для разных молекул используются разные уровни отсчета энергии. Для учета этого обстоятельства, в соответствии с уравнением
309
(XIII.4), необходимо умножить правую часть уравнения (XIII.13) на е-ΔE/RT, где ΔE - разность уровней отсчета.
Поскольку за нулевой уровень при расчете сумм состояний принимается энергия молекул при абсолютном нуле, то ΔE = -Q0,
где Q0 - теплота реакции при абсолютном нуле.
Таким образом, вместо уравнения (XIII.13) получим
Kc = (PD/PAP
)eQ0/RT.
(XIII.14)
В качестве простейшего примера рассмотрим реакцию диссоциации иода при T = 1073 K:
I2 = 21.
(XIII.15)
Согласно уравнению (XIII.14) константа равновесия этой реакции определяется уравнением
Kc = (P
/PI2)eQ0/RT
(XIII.16)
Исследование спектров атомного и молекулярного иода позволяет определить постоянные, необходимые для расчета Кc по формуле (XIII.16).
Для определения функции распределения атома иода надо знать лишь атомную массу иода (А) и величину общего момента атома:
A = 126,92; I→ = 3/2.
Для расчета функции распределения молекулы иода надо знать ее момент инерции I и частоту колебания ν:
I = 7,51·10-38 г·см2; ν = 6,39·1012 c-1.
Теплота реакции диссоциации иода при абсолютном нуле равна ∼ 150 кДж/моль.
Согласно уравнению (XIII.16), при учете уравнений § 2 этой главы
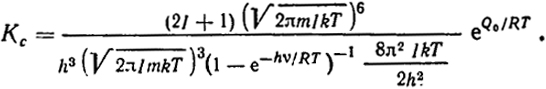 (XIII.17)
(XIII.17)
Подставив вышеприведенное значение, получим величину Kс при T = 1073К:
Kc = 7,46·1016.
(XIII.18)
В соответствии с выводом уравнения (XIII.14), концентрации в этом уравнении выражены в молекулах на кубический сантиметр.
310
Для перевода этих концентраций в обычное их измерение (моль на литр) выражение (XIII.18) надо умножить на 103 NA, а для перевода в Kp - умножить на RT.
Таким образом, получим:
Kp =
= 7,46·10
16·10
3kT = 1,1·10
-2 атм.
Зависимость изменений постоянной равновесия K диссоциации иода от температуры указывает на близость экспериментальных и расчетных величин:
| T, K . . |
1274 |
1173 |
1073 |
973 |
| Kp, атм |
1,68·10-1 |
4,80·10-2 |
1,09·10-2 |
1,80·10-2 |
311
