Статистическая механика не только дает обоснование термодинамическим методам расчета, но и позволяет связать термодинамические характеристики с микроскопическими. Из уравнения (XI.5) после подстановки B1 = 1/kT и простых преобразований получим:
300
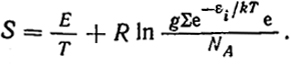
Величина Z = g
e
-εi/kT носит название суммы состояний (индекс "обл" под знаком ∑ означает, что суммирование производится по областям). Суммирование по областям и умножение на число ячеек равносильно суммированию по ячейкам. Таким образом:
Z = ∑e-εi/kT;
(XIII.1)
S =
+ Rln(Ze/NA);
(XIII.2)
A = E - TS = RTln(Ze/NA).
При рассмотрении статистики Гиббса мы ввели сумму состояний системы Q.
Z является суммой состояний молекулы.
Определим связь суммы состояний Q и Z для идеального гааа. В этом случае энергия системы складывается из энергий отдельных молекул: 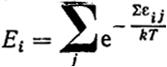 , где j - индекс суммирования молекул. Тогда:
, где j - индекс суммирования молекул. Тогда:

Однако при таком расчете мы считаем молекулы различными и поэтому каждое слагаемое в сумме считаем N! раз.
Таким образом:
Q =
.
Из уравнения A = U - TS следует, что
А = Е - TS = -kT ln ∑е-
.
Расчет термодинамических функций любой реальной системы сводится к расчету суммы состояний Q.
Точно так же термодинамические свойства идеальных газов могут быть выражены через сумму состояний согласно (XI1I.2).
A = E - TS = RTln
.
G = А + pυ = -RT ln (Ze/NA) + RT = - RT ln (Z/NA).
(XIII.3)
301
Для определения Е продифференцируем по температуре уравнение (XIII.1):
dZ/dT = ∑-εi/kT(εi/kT2).
Разделив это уравнение на уравнение (XIII.1), получим
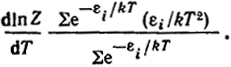
По определению

Таким образом:
ε = kT2(d ln Z/dT)
и
E = RT2(d ln Z/dT).
Мы видим, что все термодинамические функции выражаются через сумму состояний. Для того чтобы понять смысл этой характеристики, определим, сколько молекул находится в некотором состоянии j, включающем ряд областей фазового пространства:
Nj = ∑jNi.
Использовав для Ni формулу Больцмана, получим
Nj =
Отношение чисел молекул в двух состояниях j и k определяется следующим образом:
=
Сумма по областям так же неопределенна, как и величина области. Поэтому целесообразно перейти к суммированию по ячейкам. Умножив числитель и знаменатель полученного выражения на g, найдем
Nj/Nk = Zj/Zk.
Таким образом, сумма состояний определяет число молекул в данном состоянии или, другими словами, тенденцию
302
молекулы проникнуть в данное состояние. Понятно, что S растет, a F и G убывают с увеличением Z. Расчет термодинамических функций сводится к расчёту суммы состояний.
Рассмотрим два свойства суммы состояний. Если энергия молекулы равна сумме энергий отдельных видов движения, то сумма состояний равна произведению сумм состояний для этих видов движения.
Действительно, пусть
ε = ∑εj,
где j - индекс суммирования видов движения.
Тогда
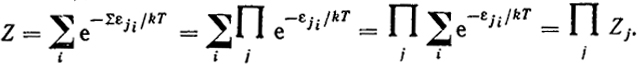
Таким образом:
Z = ZпостZврZколZэл
и расчет суммы состояний сводится к расчету суммы состояний отдельных видов движения.
Поскольку энергия ε зависит от уровня отсчета, то и значение Z зависит от этого уровня.
Как изменится Z при перемене уровня отсчета энергии на величину ε0?
Пусть величина энергии молекулы, отсчитанная от нового уровня, составит ε′, тогда
ε = ε0 + ε′
Следовательно:

Таким образом:
Z′ = Zeε0/kT
(XIII.4)
Уровень отсчета е определяет уровень отсчета F, G и Е, рассчитанных по величине Z. Величина S не зависит от уровня отсчета энергий, принятого при вычислении Z.
303
