Запас внутренней энергии идеального газа определяется числом квадратичных членов g, т.е.
E = g(RT/2).
293
Таблица XII.1. Теплоемкость и число степеней свободы
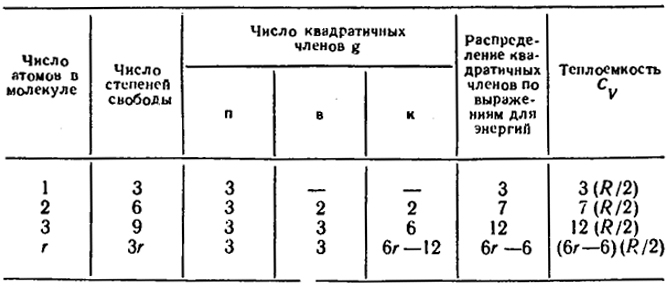
Отсюда определяется теплоемкость при постоянном объеме (табл. XII.1)
CV = dE/dT = gR/2.
В табл. XII.1 буквами "п", "в", "к" соответственно обозначены: поступательная, вращательная и колебательная энергии.
Таким образом, теплоемкость, согласно закону распределения энергии по степеням свободы, не должна зависеть от температуры.
Опыт подтверждает это для одноатомных газов.
Теплоемкость благородных газов и паров металлов равна 3 R/2 и не зависит от температуры. Лишь в случае гелия обнаружено уменьшение теплоемкости при очень низких температурах. Если r ≥ 2, то теплоемкость в противоречие с табл. XII.1 увеличивается при повышении температуры. При этом данные седьмого столбца правильно передают лишь асимптотическое значение теплоемкости при высоких температурах.
Так, все двухатомные газы имеют при высокой температуре (порядка 1000° C) теплоемкость, близкую к 29 Дж/(моль·К). Однако при комнатной температуре теплоемкость уменьшается приблизительно до 21 Дж/(моль·К), а у водорода теплоемкость уменьшается при снижении температуры, достигая 12,5 Дж/(моль·К) при температуре жидкого воздуха (90 К).
Это явление снижения теплоемкости находится в соответствии с третьим законом термодинамики (см. гл. IV), по которому CV → 0 , если Т → 0. Еще отчетливее это снижение теплоемкости проявляется для твердого тела. Мы можем рассматривать твердое тело как огромную молекулу.
294
Поскольку число атомов в грамм-атоме элемента равно числу Авогадро (NA), то число степеней свободы равно 3NA - 6, а число колебательных степеней свободы 3NA - 6, так как шесть степеней свободы относятся к поступательному и вращательному движению всего твердого тела. Пренебрегая вторым слагаемым в скобках, получим
CV = (3NA - 6)k = 3R
(XII.1)
Мы получили закон Дюлонга и Пти, по которому произведение удельной теплоемкости на атомную массу - величина постоянная для всех элементов. Поскольку измеряется не СV, а Ср, то опытная величина превышает предсказываемую уравнением (XII.1) и достигает обычно 25 Дж/(моль·К).
Опыт снова дает для теплоемкости теоретическое значение как асимптотическое при высоких температурах. С понижением температуры теплоемкость уменьшается, стремясь к нулю, при приближении температуры к 0° К.
Невыполнение закона распределения по степеням свободы явилось в свое время большой неожиданностью. Этот закон выведен на основе статистической механики и теории вероятности. Невыполнение закона распределения означает, что в аксиоматике механики что-то неверно, так как для сомнений в теории вероятности нет никаких оснований.
Как указывалось при изложении третьего закона термодинамики, уменьшение теплоемкости при понижении температуры, как и другие проявления вырождения, является следствием невыполнимости законов классической механики для микрообъектов, т.е. следствием положений квантовой механики.
295
