Задача установления распределения молекул идеального газа по областям фазового пространства сводится к рассмотрению числа способов (ωi) распределения Ni молекул, находящихся в i-той области фазового пространства, по g ячейкам. Примем, что априорная вероятность попадания в любую ячейку фазового пространства не зависит от того,
278
к каким значениям координат и импульсов она относится. Это положение представляет выражение одной из аксиом квантовой механики, утверждающей одинаковую априорную вероятность каждого квантового состояния.
Напомним, что в качестве осей фазового пространства взяты импульсы, а не скорости и что соотношение (XI.2), являющееся одним из выражений аксиоматики квантовой механики, формулируется для импульсов, а не для скоростей.
Если бы мы в фазовом пространстве в качестве осей взяли скорости, а не импульсы, одинаковым объемам отвечала бы разная априорная вероятность.
Так как каждому способу осуществления распределения молекул в одной области соответствуют все способы распределения молекул в других областях, то общее число способов равно произведению чисел способов размещения молекул в каждой области, т.е. ω = Пωi.
Определение ωi особенно просто для случая высоких температур. Очевидно, что чем выше температура, тем большей энергией обладают молекулы, тем больше их проникает в фазовые области, соответствующие высокой энергии. Следовательно, с повышением температуры плотность расселения молекул в фазовом пространстве уменьшается и при достаточно высокой температуре Ni ≪ g.
Это означает, что практически в каждой ячейке будет одна или не будет ни одной молекулы. Поэтому для случая высоких температур можно не учитывать принцип Паули, ограничивающий число частиц в одной ячейке. Этот принцип будет рассмотрен в гл. XXI.
Для определения ωi будем последовательно размещать Ni молекул по g ячейкам области. Очевидно, что каждую молекулу можно разместить, g способами, помещая в одну из ячеек. Отсюда следует, что общее число размещений равно gNi. Однако нужно учесть, что при таком расчете мы считаем молекулы отличными.
Действительно, мы считаем те размещения, при которых молекулы меняются местами. Другими словами, поскольку в каждой ячейке не более одной молекулы, то мы, учитывая их перестановки, каждое размещение считали Ni! раз. Таким образом:
ωi = gNi!Ni!
и
ω =
ω
i =
gN/
Ni!,
279
где N = ∑Ni - общее число молекул.
Для того, чтобы найти равновесное (наиболее вероятное) распределение, следует искать максимум ω при учете постоянства числа молекул N и общей энергии Е системы1:
N = ∑Ni и Е = ∑еiNi,
где ∑ берется по всем областям; εi - энергия молекулы в i-той области. Вместо максимума ω можно искать максимум энтропии S, которая монотонно растет с увеличением ω согласно уравнению
S = klnω.
Стоящая перед нами задача решается путем нахождения относительного экстремума. Отыскиваются значения Ni, отвечающие максимуму величины
S = kln(gN/
Ni!)
при дополнительных условиях: ∑Ni - N = 0
∑εiNi - E = 0.
Функция Ni! - прерывная, имеющая смысл лишь при целых значениях переменных. Для больших значений Ni можно воспользоваться формулой Стирлинга:
nNi! - NilnNi - Ni.
Таким образом:
S = k{Nlng - ∑NilnNi + N}.
(XI.3)
Для решения задачи относительного максимума следует умножить дополнительные условия на постоянные (А и В) и сложить полученные произведения с функцией, экстремум которой определяется. Это приведет к выражению,
k{Nlng - ∑NilnNi + N} + A{∑Ni - N} + B(∑Niεi - E).
Продифференцировав это выражение по Ni и приравняв результат нулю, получим
-k(1 + lnNi) + A + Bεi = 0.
Отсюда
lnNi = A1 - B1εi
280
и
Ni = A2e-B1εi
где A1, A2 и B1 - постоянные.
Для определения постоянных А2 и B1 можно использовать дополнительные условия. Мы осуществим это лишь в отношении A2:
∑Ni = N = A2
-B1εi
откуда
A2 = N/
-B1εi
Таким образом:
Ni = N(e-B1εi/
-B1εi)
(XI.4)
Число молекул, попадающих в фазовую область, отвечающую энергии εi, должно зависеть от температуры. Поэтому и величина B1 должна зависеть от температуры.
Мы могли бы ввести температуру с помощью второго дополнительного условия, связав энергию газа с температурой.
Однако рациональнее воспользоваться термодинамическим соотношением (см. гл. II)
dS = δq/T.
Из уравнений (XI.3) и (XI.4) следует:
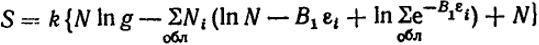
или
 (XI.5)
(XI.5)
Если объем системы постоянен, то
δqdE
и
dS = dE/T.
Из уравнения (XI.5) следует, что
dS/dE = B1k = 1/T,
откуда
B1 = 1/kTю
Таким образом, мы получаем один из важнейших законов
281
статистики - закон распределения Больцмана:
Ni = N(e-εi/kT/
-εi/kT).
(XI.6)
Величина Ni равна числу молекул в фазовой области, т.е. числу молекул, обладающих координатами и импульсами вблизи некоторых заданных значений.
Обычно представляет интерес менее детальная характеристика - число молекул Nqj или Npj. обладающих заданным (в некотором интервале) значением одной координаты (qj) или импульса (qi).
Покажем, что внешний вид формулы (XI.6) сохраняется применительно к этим задачам.
Если нас интересует число молекул (Nqj), имеющих координату qj в интервале от qj до qj + Δqj независимо от значений остальных координат и импульсов, то мы должны просуммировать выражение (XI.6) по всем импульсам и другим координатам (кроме qj):
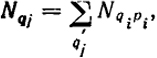
где qJ - все координаты qi, кроме qj.
Такая запись индексов суммирования обозначает, что суммирование ведется по всем импульсам (pi) и всем координатам (qi), кроме qj. Поскольку Nqipi = Ni, то
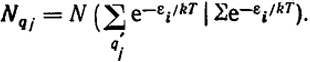
Обычно энергия выражается как сумма слагаемых, зависящих от отдельных координат или импульсов. Выделим слагаемое, зависящее от qj
ε = ε(qi) + ε(q
),
тогда
Nqj = N∑e-[ε(qi) + ε(q
)]/
kT ∣ ∑e
-εi/kT.
Так как рассматриваемая сумма произведений равна произведению сумм, то
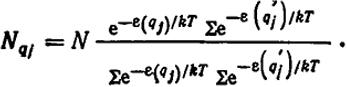
282
Следовательно:

Умножив числитель и знаменатель на Δqj и рассмотрев предельное значение знаменателя, получим
 (XI.7)
(XI.7)
Аналогично можно получить, что
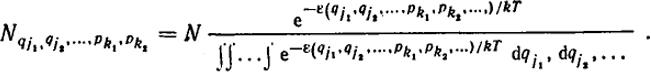
Мы рассмотрим три наиболее важных примера применения закона Больцмана.
283
1
В статистической механике внутренняя энергия, которая в термодинамике обозначалась буквой
U обозначается буквой
Е.
