Измерение э. д. с. гальванических элементов является одним из наиболее важных методов определения термодинамических свойств веществ и состояний равновесия широкого
238
круга химических реакций. Такие измерения непосредственно дают значения энергий Гиббса соответствующих реакций. Метод э. д. с. позволяет изучать металлургические равновесия в системах, содержащих металлические сплавы, оксиды, сульфиды и другие соединения. Некоторые варианты метода э. д. с. находят применение для непосредственного контроля и управления процессами сталеплавильного процесса, регулирования окисленности газовых смесей в печах для термической обработки. Рассмотрим подробно некоторые примеры использования метода э. д. с.
Определение энергии Гиббса образования химического соединения. Для определения ΔG0 силицида марганца Mn3Si5 Г.М. Лукашенко измерял э. д. с. гальванического элемента
Mnт ∣ MnCl2 в расплаве KCl - NaCl ∣ Mn3Si5, Siт.
На левом электроде происходит реакция
Мnт = Mn
+ 2
e,
а на правом электроде - образование соединения:
Mn2+ + 5/3Siт + 2у = MnSi5/3т.
Следовательно, суммарная реакция, являющаяся источником работы элемента, выражается уравнением
Mnт + 5/3Siт = MnSi5/3т.
Так как в реакции участвуют только чистые вещества и не образуется твердых растворов, то непосредственно по измеряемой э. д. с. вычисляется величина ΔG
. При 1023 K
E = 0,3846 В. Отсюда
ΔG0 = -2·0,3864·96493 = -74560 Дж/моль
(доля моля Mn3Si5ΔG0 = -74560·3 = -223680 Дж).
При помощи измерений э. д. с. рассматриваемого элемента при нескольких более высоких температурах был найден температурный коэффициент dE/dT = -1,184-4 В/К. Это позволяет вычислить изменения энтропии и энтальпии при образовании силицида марганца. Так:
ΔS
= (
nF)(d
E/d
T) = 2·96493(-1,184·10
-4) = -22,85 Дж/K·моль.
Отсюда при 1023 К.
ΔH
= Δ
G
+
TΔ
S
= -74560 + 1023(-22,85) = -97930 Дж/моль.
239
Определение активности оксидов в расплавах. Эту задачу решают с использованием твердого электролита с катионной проводимостью, например βAl2O3, содержащего небольшое количество ионов Na+ в виде Na2O. Гальванический элемент для определения активности Na2O в силикатном расплаве Са—SiO2—Na2O представлен схемой:
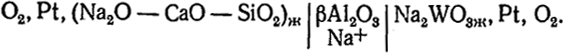
На левом электроде происходит диссоциация Na2O, и освобождающийся кислород адсорбируется на платиновом электроде. Образующиеся ионы Na+ мигрируют через твердый электролит, а электроны по металлическому проводнику переходят на второй электрод:
Na2O (Na2O - CaO - SiO2)ж = 2Na+ + 1/2O2г + 2e.
На правом электроде происходит обратная реакция, образующийся Na2O растворяется в расплавленном вольфрамате натрия:
2Na+ + 1/2O2г + 2e = Na2O (Na2WO3).
Таким образом, суммарная реакция состоит в переносе Na2O из левого расплава в правый, т.е.
Na2O (Na2O - CaO - SiO2) = Na2O (Na2WO3).
При условии, что парциальные давления кислорода на обоих электродах одинаковы:
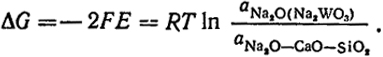
Таким образом, по величине Е можно найти отношение активностей Na2O в двух расплавах. Для нахождения aNa2O в вольфрамате натрия необходимы дополнительные данные об этой величине в расплаве CaO—Na2O—Na2O. Их можно получить каким-либо независимым путем, например из диаграммы состояния.
Определение термодинамических характеристик кислорода, растворенного в расплавленном германии. С этой целью измеряли э. д. с. гальванического элемента с твердым электролитом, в котором носителями электричества являются ионы О2-:
Oв жидк Ge ∣ ZrO2 + CaO ∣ в воздух, Pt.
На правом электроде, омываемом кислородом воздуха (pO2 ≈ 0,2), происходит ионизация О2 и его растворение
240
в платине. На этом электроде активность кислорода больше, чем на левом, который состоит из расплавленного германия, изолированного от атмосферы. Таким образом, в рассматриваемом элементе электрическая работа получается за счет переноса кислорода через твердый электролит от правого электрода к левому. Этот процесс осуществляется с помощью следующих электродных реакций:
1/2О2г + 2е = О2- правый электрод
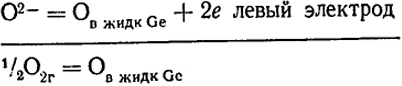
Левый электрод приобретает отрицательный заряд и, следовательно, поток электронов при работе элемента направлен слева направо. Это отвечает принятому условию записи гальванических элементов. При 1233 К и концентрации кислорода в германии cO = 27,4·10-3 % E = 0,925 В: Так как n = 2, то изменение энергии Гиббса при переносе моля ионов О2- с правого электрода на левый составляет ΔG = -2·0,925·96493 = -178500 Дж/моль.
В рассматриваемом примере целесообразно выбрать в качестве стандартного состояния кислорода в газе давление, равное 1 атм, а в расплавленном германии массовую концентрацию, равную 1 %. Подставляя в уравнение изотермы Вант-Гоффа приведенные величины cO и pO2, получим
ΔG = ΔG0 + RTln(cO/p
).
Найдем значение ΔG
:
-178500 = ΔG
+ 19,14·1233 lg
;
ΔG
= -149640 Дж/моль.
При указанной температуре были измерены э. д. с. при четырех различных концентрациях кислорода в германии. Так, при c0 = 37,2·10-3 величина э. д. с. равна 0,908В. Вычисления, подобные приведенному выше, показали постоянство ΔG
при всех четырех концентрациях кислорода. Это означает, что в указанных пределах растворы кислорода в германии являются разбавленными и подчиняются закону Генри. Поэтому для дальнейших расчетов можно вместо активности кислорода использовать его концентрацию.
241
Измерения э. д. с. описанного гальванического элемента при другой температуре (1373 K) привели к величине ΔG0 = -146540 Дж/моль. Это позволяет найти стандартные энтальпию и энтропию для процесса переноса кислорода из газа в расплавленный германий (в приближении ΔGp = 0) путем комбинирования уравнений
- 149640 = ΔH0 - 1233ΔS0;
-146540 = ΔH0 - 1373ΔS0.
Отсюда ΔH0 = -177020 Дж/моль и ΔS0 = -22,21 Дж/(K×моль). Следовательно, температурная зависимость ΔG0 определяется уравнением ΔG0 = -177020 + 22,21 Т.
Из величин ΔG0, ΔH0 и ΔS0 могут быть вычислены парциальные значения соответствующих функций для растворенного кислорода.
Кислородные гальванические элементы с твердым электролитом применяются для экспрессных определений концентраций этого элемента в жидкой стали. Они особенно важны для управления выплавкой стали в кислородных конвертерах, в которых все металлургические реакции протекают с большими скоростями. Схема такого элемента имеет вид:
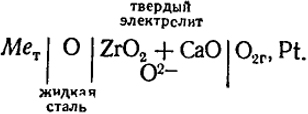
Здесь на правый электрод (вспомогательный) подается газовая смесь постоянного состава с определенным содержанием кислорода, практически это может быть воздух. Газообразный кислород, как и в предыдущем примере, адсорбируется на платине, ионизируется и переходит в имеющиеся в твердом электролите анионные вакансии. При этом от электрода отнимаются электроны и он заряжается положительно, т.е. 1/2O2г + 2e = O2-.
На левом электроде, где твердый металл (Fe, Mo или W) служит токоподводом, избыток электронов возникает в результате перехода ионов О2- в металлическую ванну: О2- = [О] + 2е. Таким образом, суммарный токообразую-щий процесс состоит в переносе кислорода из газа в жидкую сталь: 1/2О2г = [О].
Суммируя изменения химических потенциалов кислорода на электродах, найдем
Δμп = μO2- - 2μe - 1/2μO2г
242

или

где Δμ = (ψ
- 1/2μ
) может быть найдена каким-либо независимым путем. Таким образом, измеряя
Е и зная
pO2, можно найти активность растворенного в стали кислорода. Для нахождения его концентрации предварительно устанавливают связь между
aO и [О].
Перспективным является применение гальванического элемента с твердым электролитом для экспрессного или непрерывного определения концентрации кислорода в газовых смесях в различных печах с целью контроля и регулирования полноты горения топлива или использования самого кислорода. Для этого может быть использован концентрационный элемент с электродами по схеме:
| Вспомогательный электрод с точно поддерживаемой величиной pO2 |
ZrO2 + CaO |
Смесь печных газов, рO2 |
В этом случае

Попутно отметим, что такой элемент может работать как высокотемпературный топливный элемент, в котором на один электрод подается окислитель, а на другой - восстановитель.
Измерения э. д. с. применяют для определения растворимости труднорастворимых солей, например AgCl. В этом случае в насыщенном растворе произведение активностей ионов есть величина постоянная, т.е. LAgCl = aAg + aCl-. Так как раствор сильно разбавлен, то aAg+ = aCl- = mAgCl т.е. растворимость
mAgCl = √LAgCl.
Для определения LAgCl измеряется э. д. с. элемента
Ag ∣ AgClт, HCl ∣ Cl2 (pCl2 = 1 атм), Pt,
243
в котором на левом электроде ионизируется серебро: Agт = Ag+ + e, а на правом хлор: 1/2Cl2 + e = Cl- и, таким образом, суммарная реакция в элементе запишется как
Agт + 1/2Cl2г = Ag+ + Cl- = AgClт.
Э. д. с. цепи определяется уравнением
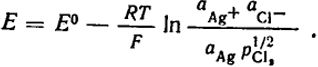
Или, так как aAg = 1 и pCl2 = 1 атм, то при 25° C
Е = E0 -
ln
aAg+ aCl- =
E0 - 0,059 lg
LAgCl.
Величина Е0 находится из табл. IX.3 как алгебраическая сумма стандартных потенциалов:
E0 = E
+
E
= -0,799 + 1,359 = 0,560 B.
Экспериментально определенная при 25° C величина E = 1,136 В, отсюда 1,136 = 0,560 - 0,059 lgLAgCl и
lgAgCl = -0,576/0,059 и LAgCl = 1,78·10-10,
или mAgCl = 1,3·10-5 г-экв/л.
Для оценки кислотности водных растворов используется величина водородного показателя, или рН. По определению эта величина представляет собой отрицательный логарифм активности ионов водорода рН = -lgaH+. Нахождение рН раствора при помощи измерения э. д. с. может быть осуществлено с использованием следующего концентрационного гальванического элемента:
Pt, H2(pH2 = 1 атм) ∣ H+(aH+ = x) ∥ H+(aH+ = 1) ∣ H2(pH2 = 1 атм), Pt,
в котором левый водородный электрод погружен в исследуемый раствор с неизвестной активностью ионов водорода, а правый электрод является стандартным водородным электродом. Как указывалось, для последнего условно принимается E
= 0. Поэтому измеряемая в опыте э. д. с. элемента равна потенциалу левого электрода, на котором происходит процесс 1/2Н
2г = Н
+ +
е.
Учитывая, что E
= 0, и переходя к десятичным логарифмам, найдем,что
E = -0,059lgaH+ = 0,059 pH.
244
В практике для определения рН стандартный водородный электрод может быть заменен каким-либо электродом-эталоном, например каломельным.
Из сказанного следует, что измерения э. д. с. подобных элементов могут быть использованы при титровании щелочей кислотами для определения точек перехода. Другой пример применения такого электрометрического метода в аналитической химии состоит в следующем.
При установлении окислительно-восстановительного равновесия между ионами разной валентности, например Fe2+ и Fe3+, потенциал инертного электрода имеет определенную величину. Если при титровании такого раствора двухромовокислым калием ионы Fe2+ полностью окисляются до Fe3+, то потенциал электрода резко изменит свою величину, и, таким образом, может быть определен конец реакции. Подобные способы, получившие широкое применение в аналитической химии, получили название потенциометрического титрования.
245
