Для вычисления э. д. с. гальванических элементов, согласно уравнению (IX.7), кроме данных о концентрациях (активностях)
231
ионов, необходимо также знание величин E0, другими словами, э. д. с. элементов при активностях, равных единице. Очевидно, для вычисления Е по активностям следовало бы иметь таблицу E0 для гальванических элементов. Однако в действительности нет необходимости составлять таблицу для всех возможных реакций и Е0. Значительно проще составить таблицу величин Е0, т.е. потенциалов электродов, измеренных относительно электрода сравнения, и при ее помощи находить Е0 для любых сочетаний пар электродов. В качестве электрода сравнения по причинам, которые будут рассмотрены ниже, выбран стандартный водородный электрод.
Таким образом, таблица стандартных потенциалов (Е0) - это по существу таблица э. д. с. элементов, состоящих из данного электрода в растворе соли с активностью, равной единице, и стандартного электрода (т.е. такого, в котором aH+ = 1 и pH2 = 1).
В элементе, состоящем из водородного и металлического электродов, происходит реакция (металл одновалентен):
1/2H2г + Me+ = Meт + H+,
(IX.23)
а цепь может быть записана следующим образом:
Pt,H2 ∣ HA ∥ MeA ∣ Me,
где МеА - соль металла; HА - кислота.
Э. д. с. этого элемента определяется уравнением
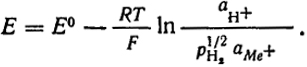
Очевидно, при aH+ = 1, aMe+ = 1 и pH2 = 1 э. д. с. равно стандартному потенциалу металла.
Таким образом, стандартным, или нормальным, потенциалом называется э. д. с. гальванического элемента, состоящего из данного электрода, погруженного в раствор, где активность ионов данного металла (или металлоида) равна единице, и стандартного водородного электрода.
Очевидно, при таком определении нормального потенциала условно принимается, что потенциал стандартного водородного электрода равен нулю. Так как при всех вычислениях э. д. с. элементов путем комбинирования величин E
потенциал стандартного водородного электрода исключается, то его абсолютная величина не имеет значения. Согласно конвенции, принятой Международным союзом по чистой
232
и прикладной химии в 1963г., стандартный потенциал определяют путем измерения э. д. с. цепи, составленной так, что стандартный водородный электрод расположен слева, а металлический (или, вообще, из любого элемента) справа.
Для определения знака потенциала учтем, что в таких гальванических элементах направление реакций окисления-восстановления зависит от природы металла, и в них может происходить как вытеснение металла водородом, так и обратный процесс. Поэтому для установления знака электродного потенциала условились всегда считать его положительным при реакциях восстановления типа (IX.23), где Ме+ приобретает электрон (восстанавливается). Если в действительности на электроде происходит окисление металла, то знак потенциала будет отрицательным.
Приведем два примера.
В цепи Pt, H2 ∣ HCl ∥ AgNO3 ∣ Ag водород вытесняет серебро, э, д. с. цепи положительна и стандартный потенциал серебра считают положительным. Здесь на правом электроде идет реакция восстановления серебра Ag+ + e → Agт и E0 = +0,799 В. Таким образом, согласно указанной конвенции, реакции записываются так, чтобы вещества в окисленном состоянии были в левой части уравнения (в данном случае Ag+), отражающего электродный процесс.
В цепи Zn ∣ ZnCl2 ∥ HCl ∣ H2, Pt в противоположность первой металл (Zn) вытесняет водород, а измеряемая э. д. с. составляет +0,763 В. Таким образом, на металлическом электроде протекает не реакция восстановления, а идет окисление, т.е.
Znт → Zn2+ + 2e.
Редакции же восстановления цинка соответствовала бы гальваническая цепь с обратной последовательностью электродов, а именно: Pt, H2 ∣ HCl ∥ ZnCl2 ∣ Zn, отвечающая отрицательному значению э. д. с. Таким образом, согласно приведенному условию, стандартный потенциал цинка, равный э. д. с. указанного гальванического элемента, отрицателен (E0 = -0,763 B).
Следует отметить, что при практических определениях величин Е
нет необходимости обязательно приготавливать растворы, в которых активности ионов в точности равны единице. Достаточно произвести измерения э. д. с. при любых концентрациях ионов водорода и металла, а затем каким-либо из описанных выше способов независимо определить активности ионов и вычислить
E0 по уравнению (IX.7). Кроме того, обычно измерения проводят не с водородным
233
Таблица IX.3. Стандартные электродные потенциалы в водных растворах при 25°С

электродом. Вместо него применяют какой-либо более удобный электрод-эталон, потенциал которого против водородного электрода хорошо известен.
Найденные подобными способами величины некоторых стандартных потенциалов приведены в табл. IX.3.
С термодинамической точки зрения, как это следует из рассмотрения реакций типа (IX.23), табл. IX.3 дает изменение энергии Гиббса при восстановлении или окислении ионов в растворах водородом. Эти изменения функции G при реакции
1/2H2г + Me
= H
+
Meт
определяются соотношением
ΔG0 = ΔG
+ Δ
G
- 1/2Δ
G
- Δ
G
.
Поскольку величины ΔG0 для простых веществ в стандартных условиях принимаются равными нулю, то ΔG0 = ΔG
- Δ
G.
Величина ΔG0 определяется из опытных данных по уравнению ΔG0 = -nE0F. Однако для нахождения ΔG
этого недостаточно, так как необходимо еще знание величины Δ
G
. Поэтому, подобно тому, как условились считать равным нулю стандартный потенциал, также приняли, что Δ
G
= 0, и тогда Δ
G0 = -Δ
G
234
Из этого следует, что табл. IX.3 эквивалентна таблице для энергий Гиббса ионов и, следовательно, может быть использована для расчетов равновесий. Очевидно, стандартная энергия Гиббса иона i определяется уравнением ΔG
= -ν
iE0F или, Δ
G
= -ν
E0F 96493 Дж (ν
i - заряд иона).
Таким образом, при помощи табл. IX.3 можно определить направление реакции в растворах. Покажем это на примере реакции окисления двухвалентного железа хлором:
Используя данные табл. IX.3 и представляя эту реакцию в виде суммы отдельных электродных реакций, найдем изменение энергии Гиббса:

Следовательно, если активности всех ионов равны единице и рCl2 = 1, то реакция пойдет слева направо. Заметим, что величина ΔG
для последней электродной реакции взята со знаком "минус", так как она написана в противоположном по сравнению с табличными данными направлением. Как уже отмечалось, все реакции, протекающие в гальванических элементах, являются процессами окисления-восстановления.
Л.В. Писаржевский одним из первых предложил считать, что вещество, теряющее электроны, окисляется, а приобретающее - восстанавливается. Так, при работе медно-цинкового элемента Zn переходит в раствор, отдавая свои электроны электроду, т.е. окисляется. При этом электрод заряжается отрицательно по отношению к раствору. Одновременно с процессом окисления цинка происходит восстановление ионов Cu2+ на медном электроде, сопровождающееся приобретением электрона.
Табл. IX.3 характеризует тенденцию металлов и металлоидов переходить в раствор в виде ионов. Металлы, стоящие в таблице выше водорода, заряжаются отрицательно
235
по отношению к водородному электроду, а ниже - положительно при условии равенства единице активностей всех ионов, участвующих в реакции. Очевидно также, что металлы, стоящие в таблице выше, являются менее благородными по сравнению с расположенными ниже и вытесняют из раствора металлы или металлоиды с меньшими значениями стандартного потенциала (при одинаковых активностях ионов). Так, например, при активностях ионов никеля и меди, равных единице, в элементе
Ni ∣ NiCl2 ∥ CuCl2 ∣ Cu
никель будет вытеснять медь.
На основании данных табл. IX.3 можно вычислить значения э. д. с. любого гальванического элемента (при 25° C) путем попарного комбинирования стандартных потенциалов. Сначала вычисляют стандартную э. д. с. элемента Е0 как алгебраическую сумму стандартных потенциалов электродов, а затем по значениям активностей электролитов находят Е.
Повторим, что в табл. IX.3 приводятся значения потенциалов как характеристики процессов восстановления, т.е. перехода ионов из раствора на электрод. Поэтому если в элементе на данном электроде происходит окисление, то следует брать значение его потенциала с обратным знаком.
Вычислим э. д. с. медно-никелевого элемента. Сначала найдем стандартную э. д. с.:
E = E
-
E
= -(-0,24) + 0,337 = 0,577 B.
При любых значениях активностей ионов э. д. с. при 25° C определится уравнением
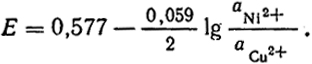
Одним из примеров окислительно-восстановительного процесса является реакция, в которой изменяются валентности ионов:
Fe2+ + Н+ = Fe3+ + 1/2H2гю
Такую реакцию можно обратимо осуществить в гальваническом элементе, где один электрод будет водородным, а другой представляет собой платиновую пластинку, погруженную в раствор, содержащий ионы двух- и трехвалентного железа. Э. д. с. построенного таким образом элемента
236
Pt, H2 ∣ HCl ∥ FeCl2, FeCl3 ∣ Pt определяется уравнением
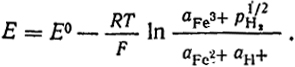
В случае, если использованный водородный электрод является стандартным (ан+ = 1 и рн+ = 1), э. д. с. элемента называется окислительно-восстановительным потенциалом электрода, и его величина выражается уравнением:
E = E0 - (RT/F)ln(aFe3+/aFe2+).
При aFe3+ = aFe2+ или при активностях ионов Fe3+ и Fe2+, равных единице, э. д. с. равна Е0, т.е. величине, которая называется стандартным (нормальным) окислительно-восстановительным потенциалом электрода. Переход металла в раствор является окислительным процессом, и, следовательно, тенденция к его самопроизвольному протеканию характеризует восстановительную способность данного металла.
Таким образом, табл. IX.3 представляет собой ряд, в котором сверху вниз уменьшается восстановительная и увеличивается окислительная способность элементов. Этот ряд называется рядом стандартных потенциалов или рядом напряжений и показывает, что элементы, у которых Е0 более отрицательны, будут проявлять себя как восстановители по отношению к элементам, стоящим ниже в этом ряду.
Какими физическими факторами определяется место элемента в ряду стандартных потенциалов?
Так как стандартный потенциал определяется изменением энергии Гиббса при реакции- взаимодействия металла (металлоида) с водородом, т.е. Меn + n/2Н2г = Meт + nH+, то ΔG0 = -nE0 96493 Дж.
Важно выяснить, из каких составных частей складывается эта величина. Для этого рассмотрим приведенную выше реакцию как ряд элементарных процессов. Учитывая, что она протекает при сравнительно низкой температуре (25° C) и оценивая величины ΔG0, приближенно можно пренебречь, изменением энтропии ΔS0 в уравнении ΔG0 = ΔH0 - TΔЫ0 и считать ΔG0 = ΔH0. Для осуществления реакции прежде всего необходимо затратить энергию D на диссоциацию молекулы водорода. Следующий этап состоит в превращении атома водорода в ион. Это сопровождается затратой энергии UH+, носящей название потенциала ионизации.
При переходе иона водорода в раствор выигрывается теплота его гидратации HH+. При одновременном восстановлении
237
иона металла сначала затрачивается энергия, соответствующая HMen+. Затем выигрывается энергия, соответствующая UMen+, при превращении иона в атом. Наконец,
выигрывается энергия, освобождающаяся при образовании кристаллической решетки из атомов, т.е. теплота сублимации а.
Таким образом:
ΔG0 = n( +
D +
UH+ -
HH+ + H
Men+ -
UMen+ + σ).
Три первые члена в этом уравнении относятся к водороду и, следовательно, одинаковы при реакциях со всеми элементами. Поэтому стандартный потенциал металла или металлоида определяется последними тремя членами уравнения. Оказывается, что наибольшее влияние на величину ΔG0 оказывает потенциал ионизации. Чем более благороден металл, тем выше его потенциал ионизации, т.е. тем труднее удалить из его атомов валентные электроны.
Энтальпия (теплота) гидратации иона зависит от его заряда и радиуса. Тенденция металлов переходить в раствор выражена тем сильнее, чем меньше потенциал ионизации и чем больше теплота гидратации. Так, наибольшим стандартным потенциалом характеризуется литий - металл с малым потенциалом ионизации. Кроме того, ввиду незначительности радиуса иона лития он имеет сильное электрическое поле и поэтому энергично притягивает дипольные молекулы воды, что сопровождается значительным выделением тепла (гидратации). Литий, таким образом, наименее благородный металл. Наиболее благородные металлы располагаются в конце ряда напряжений.
Следует, однако, заметить, что порядок элементов в ряду стандартных потенциалов существенно зависит от природы растворителя. Советские исследователи (Н.А. Изгарышев, В.А. Плесков), изучавшие гальванические элементы с неводными растворами, показали, что порядок элементов в этом ряду может совершенно измениться в зависимости от природы растворителя.
238
