Технология металлургического производства за последние десятилетия коренным образом изменяется. Широкое использование кислорода вызвало быстрое развитие конвертерного производства стали. Наряду со значительным увеличением производительности при этом способе уменьшается содержание азота, который в обычных марках стали является вредной примесью. При воздушном дутье pN2 = 0,79 (воздух содержит 79 % N2). При 1600° C равновесное содержание азота в железе [N] = 0,043√0,79 = 0,038 % (см. гл. V, закон Генри для двухатомных газов). Эта величина уменьшается при дутье, обогащенном кислородом. Если, например, оно содержит 40 % О2 и 60 % N2, то pN2 = 0,6 и [N] = 0,043√0,6 = 0,033 %.
Азот, однако, не всегда является вредной примесью. В некоторых марках нержавеющих сталей он используется как легирующий элемент.
Рассчитаем равновесные концентрации азота в легированном железе при 1600° C и рN2 = 1. Очевидно, что, при данном давлении его активность в расплаве будет такой же, как и в чистом железе. Вместе е тем присутствие атомов легирующих элементов, взаимодействие которых с азотом отличается от взаимодействия с железом, должно привести к изменению коэффициента активности азота. Это проявляется в изменении его концентрации в сплаве [N]спл по сравнению с концентрацией в чистом железе [N]Fe. При постоянстве pN2 , и, учитывая, что его раствор в железе разбавленный, получим aN = [N]Fe = f
[N]
спл.
Проведем расчеты для разбавленного раствора азота в железе, легированном Cr, Mn и Ni. Для сплава Fe-Сr-Mn в соответствии с уравнением (VI.25). aN = [N]Fe = f
×
f
[N]
спл. При практических расчетах концентрации растворенных в металле компонентов выражают в массовом содержании, % и используют десятичные логарифмы. В этом случае уравнение (VI.26) принимает вид:
lgf
=
e(j)[
j].
153
Известно, что при 1600° C в расплавленном железе е
= -0,042,
e
= -0,02 и
е
= +0,01. Таким образом, для сплава, где 80 % [Fe], 5 % [Cr], 15 % [Mn]. lg
fN = -0,042·5 - 0,02·15 = -0,51 = 1,49 т.е.
fN = 0,31.
Так как при этой температуре и pN2 = l в чистом железе [N]Fe = 0,043, то 0,043 = [N]спл·0,31 и [N]спл = 0,139. Такое увеличение содержания азота обусловлено тем, что присутствие Mn и Cr уменьшает активность азота в железе (величины e
и
e
отрицательны). В случае Ni величина
e
положительна и поэтому в присутствии этого элемента равновесная концентрация азота в железе уменьшается.
Найдем lg fN (N, Сr, Ni) и значение [N]спл при 1600° C в металле, содержащем 70 % [Fe], 5 % [Cr] и 25 % [Ni]. lg fN(N, Cr, Ni) = -0,042·5 + 0,01·25 = +0,04.
Отсюда fN = 1,1 и [N]спл = 0,043/1,1 = 0,039 %.
Легирующие элементы, имеющие большое сродство к азоту, уменьшают коэффициент его активности в железе (εN < 0), элементы же, не образующие прочных нитридов, наоборот, повышают fN(εN > 0). Такие элементы, как Si, сильно взаимодействующие с железом, также увеличивают fN.
Легирующие элементы, присутствующие в стали изменяют активности всех компонентов металлического расплава, в частности, углерода. В последнем случае это влияние качественно имеет такой же характер, как и их влияние на активность азота. Очевидно, что взаимодействие легирующих элементов с примесями должно проявляться не только в жидком железе, но и в твердых растворах на его основе. Это иллюстрируется рис. VI.4 для растворов углерода в γ-Fe (аустените). Видно, что такие элементы как Cr и Mn, которые образуют прочные карбиды уменьшают коэффициент активности углерода, в то время как Ni, не образующий в обычных условиях карбида, напротив, увеличивает aC.
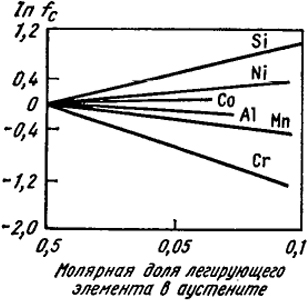
Рис. VI.4. Влияние легирующих элементов на коэффициент активности углерода в аустените при 1000° C
154
При оценке влияния легирующих элементов на активность С, N, S и других неметаллов в жидком железе следует принимать во внимание также и сродство легирующих элементов к растворителю - железу. Так, Si, образующий прочные силициды железа, повышает активность остальных растворенных веществ, как бы вытесняя их из раствора.
Процесс передела чугуна в сталь осуществляется в окислительной среде, например, в кислородном конвертере. Поэтому расплавленный металл неизбежно содержит некоторое количество растворенного кислорода (порядка 0,1 %). Растворимость же кислорода в твердом железе намного меньше и не превышает 0,01 %. Вследствие этого при кристаллизации стали образуются оксиды, выделяющиеся по границам зерен металла, что резко ухудшает его эксплуатационные свойства. Для устранения этого явления необходимо в конце плавки и при разливке по возможности полно удалить кислород из стали, т.е. раскислить ее.
Раскисление осуществляется путем добавления в сталь элементов, отличающихся большим сродством к кислороду и хорошо растворяющихся в жидком железе. Рассмотрим для примера раскисление стали алюминием, т.е. 2А1 + 3О = А12О3т.
Изменение энергии Гиббса при этой реакции
ΔG = ΔG
- (3ψ
+ 3
RT ln
аO + 2ψ
+ 2
RT ln
aA1).
При равновесии ΔG = 0, aAl2O3т = 1, поэтому
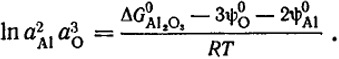
Таким образом, при T = const произведение a
a
=
LAl2O3 есть постоянная величина. В общем случае, чем более отрицательна величина энергии Гиббса образования оксида R
xO
y, тем меньше произведение активностей кислорода и раскислителя
R и, следовательно, тем ниже концентрация остающегося в железе кислорода при данном расходе раскислителя.
Алюминий является одним из наиболее сильных раскислителей стали (ΔG
при соответствующих температурах имеет порядок -1600 кДж/моль). Так как концентрации O
2 и А1 в стали малы, то вместо активностей используют концентрации. В рассматриваемом случае при 1600° C
LAl
2O
3 = [A1]
2[O]
3 = 2·10
-14 и, следовательно, при концентрации Al = 0,01 %, равновесное содержание кислорода должно быть близким к 0,0004 %. В действительности,
155
столь глубокое раскисление не достигается из-за взаимодействия стали с окислительной атмосферой и огнеупорной футеровкой.
Константа реакции раскисления стали алюминием имеет вид:  . Если продуктом реакции является чистый твердый оксид алюминия (aAl2O3 = 1), то К = 1/a
. Если продуктом реакции является чистый твердый оксид алюминия (aAl2O3 = 1), то К = 1/a
a.
Для практики имеет значение, что раскислительная способность данного элемента существенно увеличивается, если образуемый им оксид выделяется не в чистом состоянии, а в виде соединения или раствора. Например, А12О3 может образовать соединение с MnO или расплав MnO-FeO-А12О3. В этом случае aAl2O3 < 1 и соответственно уменьшится произведение а
a
. Такое образование соединений между продуктами раскисления происходит в том случае, когда используют, так называемые, комплексные раскислители, содержащие два или более элемента и с высоким сродством к кислороду. Например, распространен сплав из Al, Si и Mn, при раскислении которым образуются А1
2О
3, SiO
2 и MnO. При правильном выборе состава этого сплава указанные оксиды могут образовать легкоплавкие смеси и относительно быстро удалятся из жидкой стали, всплывая на ее поверхность.
При комплексном раскислении стали и при относительно высоких концентрациях раскислителей в точных расчетах следует учитывать параметры взаимодействия и величины f
. В рассматриваемом случае равновесие раскисления описывается совокупностью уравнений, одно из которых имеет следующий вид:
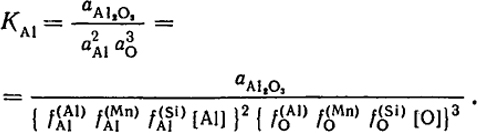
Из этого уравнения следует, что для достаточно разбавленных растворов, где fA1 и fO → l, концентрация кислорода монотонно убывает с увеличением концентрации раскислителя. Однако f
или вообще
f
уменьшается с ростом концентрации раскислителя. (Из-за малости [О] величина
f
, практически не отличается от единицы.) Поэтому при определенной концентрации раскислителя содержание кислорода в железе начинает возрастать с увеличением
156
концентрации раскислителя. Другими словами, вследствие сродства кислорода к раскислителю при больших концентрациях последнего атомы кислорода начинают сильнее удерживаться металлом в растворе, что затрудняет раскисление.
Приведенное выше рассмотрение раскисления стали алюминием справедливо лишь в пределе, когда величина энергии Гиббса образования оксида раскислителя намного более отрицательна, чем величина ΔG
. В этом случае возникающая фаза содержит только оксид раскислителя (например, только Al
2O
3). Иными словами, равновесие реакции 2[А1] + 3(FеО) = 3[Fе] + А1
2O
3т сильно смещено вправо. Естественно, что чем меньше концентрация раскислителя, тем большим может быть содержание FeO в оксидной фазе. В действительности процесс раскисления более сложен, и образующиеся продукты содержат и другие оксиды.
Отметим, наконец, что углерод также может рассматриваться как раскислитель. Особенность процесса заключается в том, что продуктом раскисления является газ (СО). Поэтому способность углерода удалять кислород из расплавленного железа сильно увеличивается при вакуумировании. Этот эффект настолько значителен, что становится возможным восстановление оксидных включений, например, SiO2T + [C] = [Si] + 2COг.
Химические реакции между элементами, растворенными в твердой стали используют для улучшения ряда ее эксплуатационных свойств. Для этого, в частности, применяют различные методы термической обработки, основанные на выделении из твердых растворов химических соединений в виде избыточных фаз. Так, выделение карбидных, карбонитридных и подобных фаз в стали в виде мелкодисперсных частиц повышает ее твердость. Например, в стали легированной ванадием при определенных концентрациях и температурах происходит выделение карбида VC: V + C = VCт.
Константа равновесия этой реакции имеет вид: K = aVC/[V][C]. Так как в этом случае выделяется чистый карбид VC, то aVC = 1 и произведение [V][C] = l/K = LVC есть величина постоянная (произведение растворимости). Зная зависимость LVC от температуры можно найти как области существования однородных твердых растворов, так и условия выделения карбида VC.
В области твердого раствора при относительно высокой температуре Т2 в обычных марках стали произведение фактических
157
(ф) концентраций ванадия и углерода меньше произведения растворимости.
При охлаждении металла до некоторой более низкой температуры (T1) произведение растворимости уменьшается и произведение фактических концентраций становится больше LVC. т.е. равновесие нарушается. Для его восстановления необходимо уменьшение [V]ф и [С]ф до значений, удовлетворяющих уравнению LVC (при T1) = [V][C]. Это осуществляется благодаря выделению из твердого раствора определенных количеств углерода и ванадия в виде карбидной фазы. По величине LVC можно вычислить количество образующейся избыточной фазы и концентрации ванадия и углерода в твердом растворе. Обозначим через х концентрацию ванадия, выделившегося в виде карбида. При равновесии с этой фазой, концентрация ванадия, оставшегося. в твердом растворе составит [V]ф - х. Учитывая атомные массы V и С (50,9 и 12,0, соответственно), выразим равновесную концентрацию углерода как [[С]ф - х(12/50,9)]. Величину х легко найти, решив квадратное уравнение:
([V]ф - x)[[С]ф - x(12/50,9)] = LVC.
Подобные процессы выделения избыточных фаз используют и для упрочнения сплавов цветных металлов. Например, широко распространены дуралюмины - сплавы алюминия, в которых упрочняющими фазами являются соединения CuА12 и Al2CuMg.
158
