Основные характеристики электрических свойств молекул - поляризуемость и дипольный момент - определяются на основе измерения диэлектрической постоянной.
Согласно формуле Клаузиуса-Моссоти, эти величины связаны следующим соотношением:
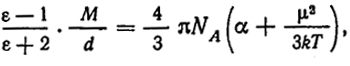 (XXV.8)
(XXV.8)
где ε - диэлектрическая постоянная среды; М - молекулярная масса; d - плотность; NA - число Авогадро; α - поляризуемость; μ - дипольный момент.
Измеряя диэлектрическую постоянную как функцию температуры, по уравнению (XXV.8) можно найти поляризуемость и дипольный момент молекулы среды. Возможно также определить поляризуемость и дипольный момент на основе измерения диэлектрической постоянной при одной температуре и показателе преломления среды п.
Формула Лоренца-Лоренца
·
=
π
NAα
позволяет непосредственно по измерению n определить α и затем по значению ε при одной температуре по формуле (XXV.8) рассчитать μ.
Поляризуемость характеризует наведенный дипольный момент μ, возникающий в молекуле под действием внешнего поля, имеющего напряженность Е (см. гл. XXIII):
μ = αE.
(XXV.9)
Размерность поляризуемости равна L3, что непосредственно
674
следует из уравнения (XXV.9):
[α] =
=
= [
L]
3.
Поляризуемость близка по величине к объему молекулы. Это следует, в частности, из следующей грубой модели. Мы будем описывать действие электрического поля на атом как сдвиг круговой орбиты (радиуса R) на расстояние Δ. На рис.. XXV.3 пунктиром показана проекция орбиты в первоначальном положении и жирной линией после включения поля.
Рассмотрим равновесие сил по оси х. Проекция центробежной силы по этой оси равна нулю. Сила, оттягивающая электрон от ядра, равна eF. Сила притяжения электрона к ядру равна e/R2 (заряд ядра принят равным заряду электрона). Проекция этой силы по оси х равна (e2/R2)cosα. Смысл обозначений R и α виден из рис. XXV.3, cosα = Δ/R. Таким образом, eE = (e2/R2)(Δ/R), отсюда μ = eΔ = R3E.
Следовательно, в соответствии c формулой (XXV.9), α = R3, если Δ мало сравнительно с R. Так как R ≈ 10-8 см, то α ≈ 10-24 см3.
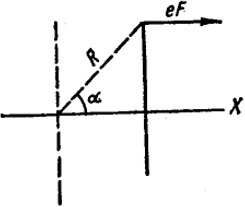
Рис. XXV.3. Схема поляризации электрона атома
Поскольку поляризуемость какой-либо атомной системы (атома, группы атомов, связи и т.д.) близка к ее объему, можно ожидать, что эта величина (и определяемая ею мольная рефракция 4/3πNAα) должны аддитивно складываться. Действительно, рефракция неорганических соединений складывается из рефракций ионов; рефракция органических молекул - из рефракций, связей, атомов или групп.
Дипольный момент так же, как поляризуемость, является характеристическим свойством данной связи. По порядку величины дипольный момент должен определяться произведением заряда электрона (10-10 эл. ст. ед.) на атомные расстояния (10-8 см).
Величина дипольного момента, равная 1·10-18 электростатических единиц, получила название одного дебая (D). Рассмотрим дипольные моменты гомологического ряда жирных спиртов. Дипольные моменты спиртов, начиная от метилового и включая такие, как С12Н25ОН, изменяются мало (от 1,60 до 1,70D). Постоянство дипольного момента
675
спиртов показывает, что он характеризует группу ОН. Дипольные моменты должны складываться как векторы.
Из дипольного момента воды можно также рассчитать дипольный момент группы ОН в воде, который оказывается равным 1,54D.
У линейных молекул (СО2, CS2) дипольные моменты связей компенсируются и общий дипольный момент равен нулю. Отличие от нуля дипольного момента H2S (0,93D), SO2 (1,61D), NH3 (1,46 D), PH3 (0,55 D) находится в соответствии с представлением о геометрической форме этих молекул, возникшим из молекулярных спектров и рентгеновского и электронного анализов. Первые две молекулы имеют треугольную форму, a NH3, PH3, AsH3 - форму треугольной пирамиды.
Векторная аддитивность дипольных моментов может быть иллюстрирована на примере дихлорбензола.
Момент связи С–Сl (определенный по дипольному моменту хлорбензола) равен 1,5 D.
Расчет результирующего дипольного момента по формуле 2μ cos α/2 (α - угол между направлениями связи С-Сl) дает для орто 2,6 D для мета 1,50 D и для пара 0D.
Отклонения векторной аддитивности могут быть вызваны различными обстоятельствами.
В ортоположении действуют стерические факторы, приводящие к увеличению α и уменьшению суммарного дипольного момента.
Водородная связь приводит к сближению положительно заряженного водорода и отрицательно заряженного кислорода и, следовательно, также к уменьшению суммарного дипольного момента. Кроме того, вообще аддитивная схема молекулы, согласно которой свойства связей остаются неизменными (см. гл. XXIII), имеет ограничения.
676
