Как указывалось выше, насыщаемость - наиболее характерная черта сил химического взаимодействия. Поэтому уже в первой работе В. Гайтлер и Ф. Лондон показали, что, в частности, атом гелия не способен к образованию связи с другими атомами.
Вообще можно показать, что энергия взаимодействия между электроном, входящим в электронную пару, и любым другим электроном определяется величиной Q - (A/2), где Q - энергия кулоновского взаимодействия, а А - обменный интеграл, как и в формуле (XXIII.10). Так как А имеет отрицательный знак, то электрон, входящий в пару, отталкивается от любого третьего электрона. Смысл и величина этого отталкивания могут быть понятны на основе следующего рассуждения. Входящий в пару электрон все время меняется направлением спина со своим соседом, поэтому с третьим электроном он также имеет как параллельное, так и антипараллельное расположение спинов в зависимости от вероятностей этих состояний.
Выше указывалось, что вероятность параллельного расположения спинов (при которой энергия взаимодействия с третьим электроном равна Q - А) в три раза больше антипараллельного (с энергией Q + A).
Таким образом, результирующая энергия взаимодействия электрона пары с третьим электроном
1/4(Q + A) + 3/4(Q - A) = Q - (A/2).
(XXIII.11)
Таким образом, между атомами (или молекулами) с замкнутыми оболочками имеет место отталкивание. Это отталкивание и определяет радиусы систем с замкнутыми оболочками.
В § 2 было принято, что зависимость энергии этого отталкивания от расстояния описывается степенной функцией. Квантово-механические расчеты показали, что лучшим приближением по сравнению со степенной функцией является более сложная функция.
Отталкивание насыщенных молекул точно так же, как и отталкивание атома от насыщенной молекулы, приводит к появлению энергии активации. Рассмотрим этот вопрос несколько подробнее для случая взаимодействия атома B1 с молекулой В2В3 с образованием молекулы B1B2 и свободного атома В3.
Квантово-механический расчет приводит к следующей
603
формуле для энергии взаимодействия трех атомов:
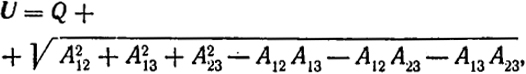 (XXIII.12)
(XXIII.12)
где Q - кулоновская энергия; Aik- обменный интеграл между двумя атомами Bi и Bk.
Если расстояние первого атома (B1) от первых двух велико, то, так как A12 = A13 = 0, формула (XXIII.12) переходит в формулу (XXIII.10):
U = Q + A23.
При приближении первого атома к молекуле В2В3 имеет место отталкивание его от молекулы. Для больших расстояний атома от молекулы можно считать, что А12 и А13 значительно меньше A23. Пренебрегая квадратом этих малых величин, получим
U = Q + A23 - (A13/2) - (A12/2).
Эта формула находится в соответствии с формулой (XXIII.11). Атом B1 отталкивается от обоих электронов пары молекул В2В3. Энергия активации нужна для преодоления этого отталкивания.
По мере приближения атома B1 расстояние В2В3 увеличивается. Энергия системы в соответствии с формулой (XXIII.12) и путь реакции показаны на рис. XVI.6. Мы ограничимся здесь простейшей, данной Ф. Лондоном, оценкой энергии активации. Пусть атом B1 приближается к молекуле В2В3 по линии связи со стороны В2. Тогда расстояние B1B3 существенно больше В1В2. Поэтому будем полагать /4i3 = 0. Тогда
U = Q + √A
+ A
- A12A23.
(XXIII.13)
Примем в этой приближенной оценке, что расстояние В2В3 постоянно. Тогда U зависит от расстояния В1В2. Пренебрежем, кроме того, кулоновской энергией Q. Тогда U меняется лишь потому, что с расстоянием В1В2 меняется A12. Чтобы найти максимальное значение энергии системы энергию переходного состояния), необходимо приравнять нулю ∂U/∂A12 при A23 = const:

Отсюда A12 = A23/2.
604
Подставив эту величину в уравнение (XXIII. 13), получим
U = Q + (√3/2)A = Q + 0,85A.
Таким образом, энергия рассматриваемой конфигурации изменилась от значения А (расстояние В1В2 равно бесконечности) до значения 0,85 А (переходное состояние). Отсюда следует, что энергия активации составляет около 15 % от энергии связи. Результат этого приближенного расчета близок к результатам точного расчета по формуле ;(ХХIII.12) (см. рис. XVI.6).
605
