Открытие Д.И. Менделеевым периодического закона осветило развитие химии и ряда разделов физики на многие десятки лет. Д.И. Менделееву удалось обнаружить важнейший закон, являющийся непосредственным следствием волновых свойств вещества и соединяющий ранее разрозненные свойства элементов в стройную систему.
Согласно этому закону, многие свойства элементов являются периодической функцией их атомной массы. Это относится, в частности, к валентности, атомным объемам, потенциалам ионизации и ко многим другим свойствам, например коэффициентам линейного расширения, сжимаемости и др. При этом в ряду элементов, расположенных по возрастанию атомной массы, элементы со сходными свойствами периодически повторяются (см. рисунок на форзаце).
Иногда открытие Д.И. Менделеева сравнивают с решением задачи установления правильной последовательности ранее перепутанных клавишей рояля. Однако следует учесть, что к моменту открытия периодического закона многих "клавишей" не доставало, так как были известны только 63 элемента из 92, существующих в природе. Кроме того, многие "клавиши" издавали фальшивые звуки. Менделееву пришлось сильно изменить принятые в то время атомные массы ряда элементов. Так, атомные массы урана и тория он полагал равными 232 и 240 вместо принятых значений 116 и 120. Атомную массу церия Менделеев рекомендовал считать равной 138 вместо 92.
Кроме того, сама периодическая функция, описывающая изменение свойств с атомной массой, сложна. Величины промежутков между атомами с близкими свойствами (периоды) не одинаковы. В первом периоде только два элемента (Н и Не), во втором 8 (от Li до Ne), в третьем снова 8 (от Na до Аr), в четвертом 18 (от K до Kr), в пятом снова 18 (Pb–Xe), в шестом 32 (Cs–Rn); седьмой период не достроен.
Числа, определяющие размеры периодов (2, 8, 18, 32), описываются законом 2n2, где п = 1, 2, 3, 4 ...
Сложность периодического закона определяется также и тем, что в одном месте таблицы на значительном отрезке изменения атомной массы свойства элементов практически
576
не изменяются. Четырнадцать редкоземельных элементов имеют одинаковую валентность и очень близкие свойства.
Трудность открытия периодического закона в XIX столетии определялась также и тем, что тогда не было известно, что атом состоит из заряженных частиц. Д.И. Менделеев искал независимую переменную, отправляясь от законов механики, полагая, что масса атома должна определять его свойства.
Атом был "электрифицирован" лишь через несколько десятков лет, и тогда стало ясно, что эти свойства должны зависеть прежде всего от числа электронов и, следовательно, от равного этому числу заряда ядра.
Периодический закон мог быть открыт так рано лишь потому, что между зарядом ядра и атомной массой существует простая связь. Так, в начале таблицы отношение атомной массы атома к заряду его ядра приблизительно равно двум.
Как уже отмечалось ранее, кроме того, могут существовать атомы с различной атомной массой и одинаковым зарядом. Такие атомы называются изотопами. Природные элементы представляют собой обычно смесь изотопов. Так, например, кислород представляет собой смесь трех изотопов с атомными массами 16, 17 и 18.
Если расположить изотопы всех элементов по возрастанию атомной массы, то периодический закон будет значительно труднее обнаружить. Так, в частности, в одной клетке окажутся атомы различных элементов с одинаковыми атомными массами (ибозары).
Д.И. Менделееву не была известна истинная независимая переменная (заряд ядра), и ему пришлось расположить элементы в нескольких местах таблицы вопреки принятому принципу возрастания атомной массы.
В таблице, охватывающей все известные в настоящее время элементы, в трех местах не выполняется принцип возрастания атомной массы. Действительно, Ar предшествует К, хотя атомная масса Ar выше, чем K. Точно так же Co предшествует Ni, а Те - I.
Несмотря на все это, Д.И. Менделеев не только открыл периодическую закономерность, но и понял, что эта закономерность представляет важнейший закон, ЧТОБ ней проявляются фундаментальные свойства вещества, и это дало ему возможность уверенно предсказать свойства новых, еще не открытых элементов, что справедливо было отмечено Ф. Энгельсом как научный подвиг. Эти предсказания блестяще оправдались. Так, например, для галлия, названного
577
Д.И. Менделеевым экваалюминием, он предсказал следующие значения свойств: атомная масса 68, плотность 5,9 - 6, атомный объем 11,5. Оказалось, что у галлия атомная масса равна 69,7, плотность 5,96 и атомный объем 11,6. Дальнейшее развитие химии и физики позволило подвести теоретическую базу, объяснить периодический закон, вывести его как следствие законов, описывающих элементарные свойства вещества.
Прежде всего, после опытов Э. Резерфорда и установления нуклеарной модели атома стало ясно, что масса атома не играет непосредственно существенной роли в определении химических свойств элементов. Было очевидно, что число электронов атома и характер орбит должны определяться зарядом ядра атома. уже опыты Э. Резерфорда позволили оценить величины зарядов ядер.
Однако наиболее общий и простой метод определения зарядов ядер был дан Мозли на основе изучения спектров рентгеновских лучей. Рентгеновские волны обладают меньшей длиной волны по сравнению с видимым светом, большей частотой и, следовательно, их кванты обладают большей энергией. Они возникают в результате переходов электронов внутренних оболочек атомов. Эти электроны крепче связаны и находятся, следовательно, на более низких энергетических уровнях. Рентгеновское излучение обычно вызывается воздействием на вещество потока электронов, которые выбивают внутренние электроны атомов. На освободившиеся места приходят электроны, находящиеся на более высоких энергетических уровнях. При этом выделяются кванты рентгеновского излучения.
Рассмотрим частоты рентгеновских лучей, возникающих в случае выбивания электрона с квантовым числом n = 1 (K-электрона).
Согласно принципу Паули, таких электронов может быть два. Обладая одинаковыми значениями первых трех квантовых чисел, они будут иметь антипараллельные спины (направленные в противоположные стороны). Таким образом, после того как один электрон из K-оболочки будет выбит, второй будет экранировать ядро, эффективный заряд которого будет, следовательно, не Z, a Z - 1.
Тогда излучение при переходе электрона с главным квантовым числом п = 2 на K-оболочку опишется формулой:
ν =
(
-
)
578
или
ν =
·
.
Таким образом, (Z - 1) ∼ √ν.
Это соотношение было найдено как эмпирическое Мозли. Оно позволяет по частоте рентгеновских лучей ν определять заряд ядра. Z. После того как этим способом были определены заряды ядер различных элементов, оказалось возможным принять заряд ядра за порядковый номер в таблице.
При расположении элементов по возрастанию заряда их ядер не возникают те исключения, которые возникают, как указывалось выше, при расположении по возрастанию атомной массы. Действительно, заряд ядра Ar (18) оказывается меньше, чем у К (19); у Со (27) меньше, чем у Ni (28), а у Те (52) меньше, чем у I (53).
Все изотопы попадают в одну клетку таблицы, так как ядра их атомов обладают одинаковым зарядом и, следовательно, они имеют одинаковый порядковый номер.
Замена атомной массы зарядом ядра была первым шагом в раскрытии физического смысла периодического закона. Далее, было важно установить причины возникновения периодичности, характер периодической функции зависимости свойств от заряда ядра, объяснить величины периодов, число редкоземельных элементов и пр.
Заслуги в разработке этого важного этапа развития периодического закона принадлежат Н. Бору. Он показал, что периодический закон Д.И. Менделеева является следствием волновой механики и принципа Паули.
Периодичность в физике почти всегда является проявлением волновых свойств. Мы видим (§ 4), что для электрона устанавливается определенный набор состояний, описываемых квантовыми числами. Принцип Паули определяет распределение электронов по этим состояниям.
Мы можем пользоваться выведенными для водорода четырьмя квантовыми числами для описания состояния электронов в любом атоме лишь в рамках описанного выше приближенного рассмотрения отталкивания электронов. Будем, как и ранее, полагать, что это отталкивание сводится к экранированию ядра. В этом случае каждый электрон может быть описан как водородоподобный, поскольку заряд ядра уменьшен остальными Z - 1 электронами до единицы.
Таким образом, электронам представляются квантовые состояния, описываемые квантовыми числами п, I, m, σ.
579
Рассмотрим заполнение этих состояний в различных атомах начиная от водорода. Электрон водорода в основном состоянии характеризуется n = 1, l = 0 и m = 0. Это 1s-электрон.
Переход к следующему атому таблицы Д.И. Менделеева (гелию, Z = 2) мы осуществим, добавляя второй электрон и требуя, чтобы он занял самое низшее энергетическое состояние, не противоречащее, однако, принципу Паули.
При этом оба электрона в рамках принятого приближения можно описать четырьмя квантовыми числами атома водорода, так как для каждого из них экранизированный заряд ядра равен +1.
Таким образом, в основном состоянии атом гелия имеет 2 электрона Не(1s)2.
Как уже упоминалось (см. § 4), пара электронов с насыщенными спинами не обладают химической валентностью. Таким образом, после водорода, валентность которого равна единице, следует гелий, обладающий валентностью, равной нулю, и являющийся благородным газом.
Так как если n = , то l = 0 и, следовательно, m = 0, то принцип Паули не позволяет большему числу электронов располагаться в первом периоде, и третий электрон (в атоме Li Z = 3) должен иметь n = 2. Таким образом, в соответствии с опытом, в первом периоде периодической системы располагаются лишь два элемента. Литий начинает второй период. Два из его электронов заполняют гелиевую оболочку, но третий занимает состояние 2s: Li (1s)2 (2s)1.
Мы видим, что литий, как и водород, является одновалентным. Следующий атом - Be (Z = 4) в согласии с принципом Паули характеризуется следующими квантовыми числами: (1s)2(2s)2. В этом основном состоянии валентность бериллия равна нулю. Однако значению n = 2 отвечает не только l = 0 (электронов), но и l = 1.
Энергия возбуждения в состоянии с увеличением главного квантового числа велика по сравнению с энергией химического взаимодействия, и поэтому атом гелия, например, никогда не имеет двух валентностей, так как затрата для перехода в состояние (1s) (2s) не скомпенсируется выигрышем энергии при химическом взаимодействии.
Энергия возбуждения в состоянии, отвечающем тому же главному квантовому числу, но другому побочному, меньше энергии, выигрываемой при химическом взаимодействии, и поэтому такое возбуждение возможно. Вследствие этого бериллий может участвовать в химических реакциях в состоянии Be(1s)2 (2s)1 (2p)1, обладая валентностью, равной
580
двум. Такая валентность, возникшая в результате возбуждения электрона, носит название q-валентности.
Следующий атом бор (Z = 5). В соответствии с принципом Паули его электроны распределяются следующим образом: B(1s)2(2s)2(2p)1.
Таким образом, в основном состоянии бор одновалентен, но один 2s-электрон, как и в случае бериллия, может перейти в 2р-состояние. Бор в состоянии (1s)2(2s)2(2р)2 обладает валентностью, равной трем, так как р-электрону отвечают различные значения магнитного квантового числа m и, электроны могут расположиться с параллельными спинами в р-состоянии, не вступая в противоречие с принципом Паули. Следовательно, бор может иметь валентность, равную трем. Известно, что бор действительно обладает в различных соединениях двумя указанными валентностями: 1 и 3.
При рассмотрении расположения электронов следующего атома - углерода (Z = 6) снова следует учесть, что для l = 1 возможны три значения магнитного квантового числа т, а именно:-1; 0; +1. При этом в отсутствие внешнего поля энергия электрона не зависит от m. Не нарушая принципа Паули, мы можем иметь в одном шесть 2р-электронов, так как в каждое состояние с заданными l и m можно помещать два электрона с антипараллельными спинами. Схематично состояния, которые представляются электронам углерода, показаны на рис. XII.6.

Рис. XXII.6. Схема расположения электронов атома углерода
Мы видим, что 2р отвечают три состояния, которые схематично изображены разными линиями, хотя энергетически они эквивалентны. Очевидно, что 1s - 2s-электроны должны иметь антипараллельные спины, чтобы удовлетворять принципу Паули. 2р-электроны могут расположиться так, как указано на рис. XXII.6, с параллельными спинами, либо обладать одним значением m и тогда иметь антипараллельные спины.
Гунд установил эмпирическое правило (позднее оно было теоретически обосновано) наибольшей мультиплетности. Внутри одного атома при данных значениях п и l электроны стремятся иметь параллельные спины и поэтому наибольшую валентность и, следовательно, мультиплетность. Если бы не это обстоятельство и не наличие q-валентности,
581
валентность всех атомов равнялась бы нулю или единице. Поэтому углерод в основном состоянии двухвалентен, но в состоянии (1s)2(2s)1(2p)3 он обладает валентностью, равной четырем. В соответствии с правилом Гунда азот N(1s)2(2s)2(2p)3 имеет валентность, равную трем, но ион азота N + (1s)2(2s)(2р)3 имеет валентность, равную четырем, и подобен четырехвалентному углероду. Кислород O(1s)2(2s)2(2p)4 должен обладать, в соответствии с принципом Паули, валентностью, равной двум, фтор F(1s)2(2s)2(2р)5 - валентностью, равной единице, и неон Ne(1s)2·(2s)2(2p)6 должен обладать валентностью, равной нулю. На этом благородном газе оканчивается второй период периодической системы. Мы видим, что, в соответствии с опытом, он содержит 8 элементов.
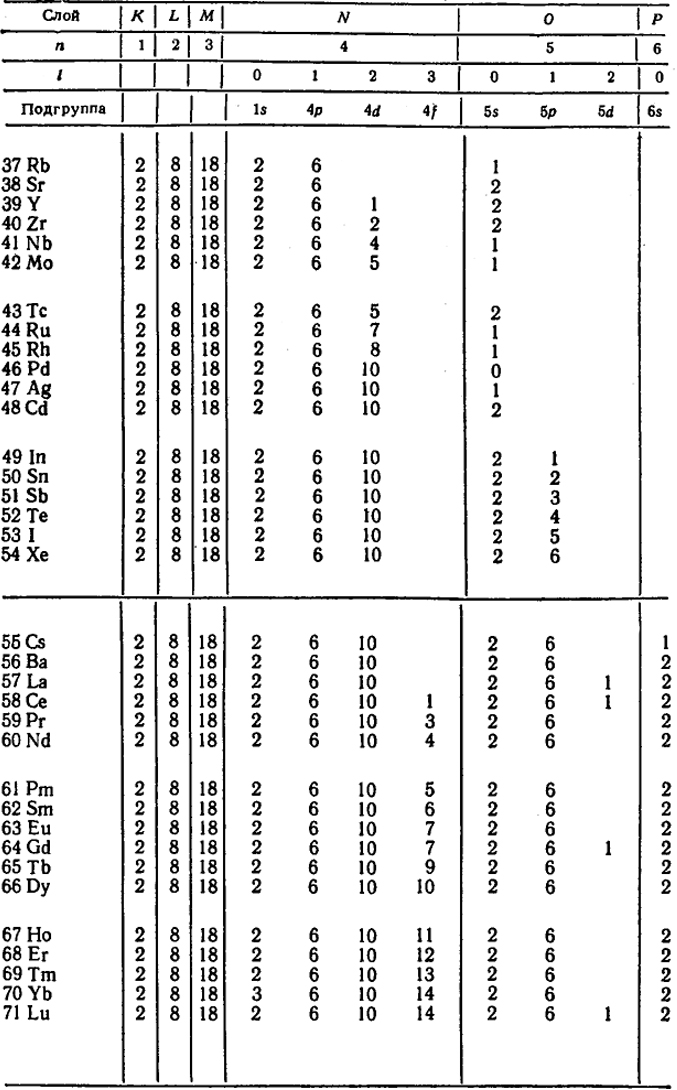
Характеристики квантовых чисел электронов элементов даны в табл. XXII.1.
Определим в общем случае число электронов (Nn), которые могут обладать данным значением квантового числа, т.е. число элементов, находящихся в n-ном периоде таблицы.
Мы знаем, что квантовому числу п отвечает п значений побочного квантового числа l (от 0 до п - 1), при этом каждому значению l отвечает 2l + 1 значений магнитного квантового числа т.
Поэтому
Nn = 2
l (2
l + 1).
Множитель 2 перед суммой возник потому, что каждой тройке значений n, l и m отвечают два электрона с антипараллельными спинами.
Таким образом:
Nn = 4
l + 2
l.
Первая сумма представляет собой арифметическую прогрессию, а вторая просто равна п (содержит п единиц). Таким образом:
Nn = 4
+ 2n = 2n2.
(XXII.32)
Мы видим, что ранее сформулированная закономерность в величинах периодов вытекает непосредственно из квантовой механики. Однако, согласно формуле (XXII.32),
582
Таблица XXII.1. Распределение электронов в атомах

583
Продолжение табл. XXII.1
584
Продолжение табл. XXII.1

585
в третьем периоде должно быть 18 элементов. Между тем, как указывалось выше, третий период содержит, как и второй, лишь 8 элементов. От натрия (Z = 11) до аргона (Z = 18), как это видно из табл. XXII.1, заполнение происходит совершенно так же, как и во втором периоде от лития до неона.
Таким образом, электроны Ar целиком заполняют 3p-состояния. Далее, казалось, должна была заполняться 3d-oбoлочка. Кроме того, наличие d-оболочки должно было вызвать q-валентность у аргона, который, следовательно, не должен был обладать свойствами инертного газа.
Однако многочисленный опыт показывает, что 3d-coстояния оказываются энергетически значительно выше не только 3p-состояния, но и 4s-состояния. Действительно, вслед за 3p-оболочкой начинает заполняться не 3d-, a 4s-, и 3d-состояния остаются незаполненными.
Мы видим по табл. XXII.1, что у калия вслед за шестью 3p-электронами заполняется 4s-состояние. Поэтому калий, подобно натрию и литию, является щелочным металлом и начинает четвертый период. То, что состояние, отвечающее четвертому главному квантовому числу (4s), оказывается ниже состояния, отвечающего третьему главному числу (3d), показывает неточность принятого приближенного описания отталкивания электронов. Если картина экранирования была бы точной, то уровень 4s должен быть значительно выше уровня 3d. Электрон на орбите 4s меньше отталкивается от электронов оболочки с главным квантовым числом 3 по сравнению с электронами 3d. У атома кальция завершается заполнение 4s-оболочки. Начиная от Sc начинается заполнение ранее "пустовавшего" 3d-состояния. Таким образом, наряду с шестью 3р-электронами Sc имеет два 4s- и один 3d-электрона.
Начиная от Sc в последующих элементах происходит заполнение 3d-состояния. У титана, следующего за скандием, два 3d-электрона, у ванадия 3, у марганца 5, а у железа 6. Таким образом, электроны железа опишутся следующим образом: Fe(1s)2(2s)2(2p)6(3s)2(3p)6(3d)6(4s)2.
Атом кобальта обладает семью 3d-электронами, а никеля - восемью. В следующем за никелем атоме меди оказывается сразу 10 3d-электронов. Одному 4s-электрону оказывается выгодно перейти в 3d-состояние, чтобы полностью заполнить третью оболочку.
Таким образом, распределение электронов меди опишется следующим образом: Cu(1s)2(2s)2(2p)6(3s)2(3p)6(3d)10(4s)1.
586
У цинка два 4s-электрона. Начиная от галлия происходит заполнение 4р-состояния, которое завершается у Kr. После этого у Rb электрон вместо 4d(-состояния занимает 5s-состояние. Таким образом, четвертый период завершается на криптоне и содержит 18 элементов начиная от K(Z = 19) до Kr(Z = 36).
Элементы начиная от Sc(Z = 21) и до Cu(Z = 29) содержат незаполненное 3d-состояние. Эти элементы в табл. XXII.1 выделены. Атомы с незаполненными оболочками обладают многими общими чертами. Наличие свободных мест с близкой энергией приводит к возможности осуществления различных расположений электронов, отвечающих различной валентности атома. Атомы переходных элементов обладают, таким образом, переменной валентностью.
Наибольшая валентность может быть осуществлена у марганца, когда все 3d-электроны занимают разные ячейки, а один из 4s-электронов переходит в состояние 4р. При этом валентность равна семи.
Наличие большого числа возможных распределений электронов по d-состояниям приводит к большому числу энергетических состояний и, следовательно, к малым значениям энергий перехода из одного состояния в другое.
Атомы переходных элементов способны, следовательно, поглощать малые кванты энергии. Это приводит к тому, что переходные элементы поглощают (и испускают) свет в видимой части спектра. Поглощение в видимой части спектра означает наличие цвета у тела как в отраженном, так и в проходящем свете.
Незаполненные электронами 3d-состояния могут привлечь неразделенную пару электронов какой-либо молекулы. Это приводит к способности переходных элементов давать комплексные соединения. Известно, например, что железо образует тетра- и пентакарбонилы. Жидкий карбонил железа может быть разогнан и отделен от примесей. На этой основе построен один из промышленных методов получения весьма чистого железа.
Наконец, электроны атомов переходных элементов, располагаясь по одному в различных d-ячейках, могут иметь одинаково направленные спины и, следовательно, приводить к высоким значениям спинового и магнитного моментов. Таким образом, для переходных элементов должно быть характерно наличие собственных магнитных моментов и, следовательно, высоких значений магнитной восприимчивости.
Из табл. XXII.1 видно, что после стронция начинается
587
заполнение 4d-ячеек, точно так же, как после кальция осуществлялось заполнение 3d. Заполнение 4d-состояний завершается у палладия. В следующем после палладия атоме серебра сорок седьмой электрон, "игнорируя" наличие свободной 4f-оболочки, занимает состояние 5s. Состояние 4f оказывается энергетически столь невыгодным, что после заполнения 5s-состояний (у кадмия) начинается (у индия) заполнение 5p-оболочек, которое завершается у ксенона. Таким образом, в пятом периоде оказывается 18 элементов (от Z = 37 до Z = 54).
У атома цезия начинает заполняться 6s-состояние, а у атома бария это заполнение завершается. У следующего за барием лантана начинает заполняться 3d-оболочка. Таким образом, у этих атомов оказываются незаполненными не только предыдущий (пятый) "этаж", но и в четвертом остаются свободными 14 мест 4f-ячеек. И вот после лантана начинают заполняться эти далеко находящиеся от внешних электронных оболочек орбиты. Естественно, что элементы, в которых происходит заполнение f-ячеек, по своим свойствам весьма близки к лантану. Они также трехвалентны. Эти элементы носят название лантонидов, или редких земель. Остановимся кратко на все возрастающем применении редких земель.
Небольшие добавки редких земель к сталям улучшают ряд их свойств, в частности пластичность, особенно при низких температурах. Присадка редких земель к хромоникелевым сплавам повышает их жаропрочность. Добавка сотых процентов редких земель позволяет получать высокопрочный чугун с шаровидным графитом. Редкие земли используются при выплавке стали как раскислители, дегазаторы и десульфураторы. Особенно велико применение редких земель в атомной технике.
Атомная техника потребовала много новых материалов с заданными свойствами. Редкие земли используют и в специальных стержнях для регулирования и аварийной защиты реакторов, а также в самых различных направлениях (атомные электрические элементы - на прометрии 147, портативные рентгенопросвечивающие аппараты - на тулии 170 и пр.). Значительную часть продуктов деления урана и плутония составляют редкие земли.
Следует отметить, что в то время, когда Н. Бор строил таблицу, семьдесят второй элемент не был открыт. Было неясно, сколько должно быть редких земель. Полагая, что число их равно пятнадцати, семьдесят второй элемент искали среди минералов, содержащих редкие земли. Так как
588
число 4f-электронов равняется 14, то этот элемент должен иметь близкую к цирконию внешнюю оболочку. Поэтому Н. Бор предложил искать семьдесят второй элемент в циркониевых рудах. Этот элемент, названный гафнием, и был обнаружен в циркониевых рудах. Цирконий и гафний играют большую роль в современной атомной технике. В частности, интенсивно поглощающий нейтроны гафний должен быть удален из циркония, употребляемого на изготовление труб, по которым циркулирует теплоноситель в котлах атомных электростанций.
Заполнение 3d-оболочки заканчивается у золота, а заполнение 6р - у радона, который завершает шестой период периодической системы. Этот период содержит, таким образом, тридцать два элемента (от Z = 55 до Z = 86). Он содержал бы, как и предыдущий период, 18 элементов, если бы в него не входили четырнадцать элементов редких земель, в которых происходит заполнение электронами мест в 4f-состояниях.
Седьмой период начинается искусственно синтезированным (отсутствующим в природе) последним щелочным металлом францием, внешний электрон которого располагается в 7s-состоянии.
Внешняя оболочка радия подобна таковой у бария, а актиния - оболочке лантана. За актинием начинаются актиноиды, которые заканчиваются на 103-м элементе - лоуренсии. Электронная оболочка 104-го элемента курчатовия подобна оболочке гафния.
589
