В природе уран существует в двух степенях окисления: +4 и +6. В лабораторных условиях получены слабоустойчивые U (III) и U (V).
Уран (IV) в своих соединениях присутствует в форме иона U4+. По химическим свойствам он близок к Th (IV), Y (III) и тяжелым лантаноидам иттриевой группы. С химической точки зрения ион U4+ является слабым основанием. Он существует лишь в сильнокислых растворах и при понижении кислотности гидролизуется с образованием U(OH)4. Гидроксид U(OH)4 слаборастворим в воде, но хорошо растворяется в кислотах. Диоксид урана UO2 практически не реагирует с водой до 300°С, нерастворим в НСl, но хорошо растворяется в HNO3 и смесях кислот. Из соединений U (IV) наиболее растворимы в воде UC14 и U(SO4)2. Вследствие этого U (IV) устойчив в сильнокислых сульфатных, хлоридных и нитратных растворах. Силикаты U (IV) растворимы в сильнокислых средах. U (IV) склонен к образованию комплексных соединений, где имеет координационное число 8. Известны карбонатные, сульфатные, оксалатные и другие комплексы U4+. Большинство из них малоустойчиво, причем устойчивость падает с повышением температуры. Например, в карбонатных растворах U (IV) образует устойчивый в избытке карбоната комплекс U(CO3)
.
Уран (VI) - наиболее устойчивая степень окисления урана при свободном доступе воздуха. Валентность 6 является высокой даже для такого крупного катиона, как U6+. Он энергетически неустойчив и в водных растворах мгновенно гидролизуется с образованием комплексного двухвалентного катиона уранила UO
. Например, UF
6 + 2Н
2О → UO
2F
2 + 4HF.
44
По размерам уранил-ион превышает все известные в природе катионы и равен 2,64 · 6,84 Å (Макаров, 1973). В связи с этим ион UO
не может изоморфно замещать другие катионы в химических соединениях и в природе легко образует собственные минералы.
UO3 - весьма активное химическое соединение. Взаимодействуя с кислотами, образует растворы солей уранила. По представлениям Е.С. Макарова, в минералах (уранинитах, настуранах) UO3 находится в виде уранильных групп, где для компенсации положительного заряда в пустоты решетки внедряются ионы О2- : UO
· О
2 = UO
3. Соединения U(VI) сравнительно хорошо растворимы и устойчивы в водных растворах. Наиболее растворимы уранил-нитраты. Хорошо растворимы сульфаты уранила и оксигалогениды (UO
2Cl
2 и UO
2F
2). UF
6 и UCl
6 летучи, но в присутствии паров воды легко гидролизуются, переходя в оксигалогениды. Растворимы многие соли уранила с органическими кислотами. Важнейшими труднорастворимыми соединениями U (VI) являются фосфаты, арсенаты, ванадаты.
U (VI) проявляет большую склонность к образованию комплексных соединений, которые играют огромную роль в его геохимии. Во всех этих соединениях уран находится в форме уранил-иона, который имеет координационные числа 4 и 6. Комплексообразование U (VI) с Сl-, Вr- и NO-3 идет слабо. Наиболее важное значение в природных условиях имеют карбонатные, сульфатные, фторидные, фосфатные и гидроксокомплексы. Аквагидроксокомплексы уранила образуются при ступенчатом замещении аквагрупп в акваионе уранила [UO2(H2O)6]2+ и имеют форму [UO2(OH)n(H2O)6-n]2-n (n - от 0 до 6) (Наумов, 1978).
Карбонатные комплексы образуют семейство соединений, среди которых в водных растворах устойчивы лишь [UO2(CO3)3]4- и [UO2(CO3)2(H2O)2]2-. Первый преобладает в растворе с избытком ионов СО
и при разбавлении переходит во второй. Следующей ступенью является образование слаборастворимого карбоната уранила UO
2CO
3 (рис. 3.1). Фторидные комплексы образуются лишь в средах с высокими концентрациями фтора. Так, для 25°С пороговая концентрация фтора должна составлять 0,5 мг/л (Наумов, 1978). Сульфатные комплексные соединения уранила по строению подобны карбонатным, однако по прочности уступают не только карбонатным, но и фторидным. Они характерны лишь для кислой среды с рН 2 - 4 (рис. 3.2). Очень важную группу комплексных соединений уранил-ион образует с органическими кислотами (щавелевой, уксусной, лимонной, группой гумусовых кислот и т.д.).
45
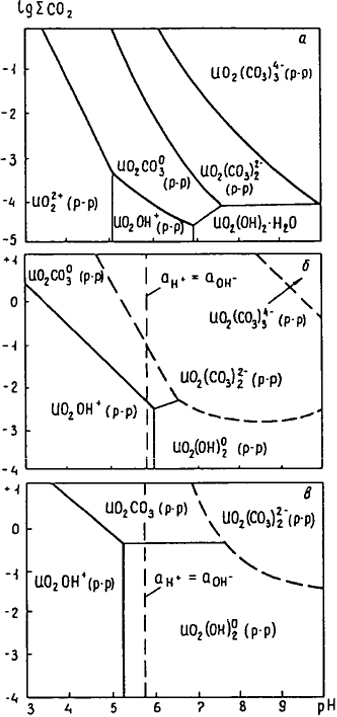
Рис. 3.1. Соотношение полей преобладания различных ионов уранила в координатах lg ∑ CO
2 при 25°С (
а), 150°С (
б), 300°С (
в) (
Наумов, 1978)
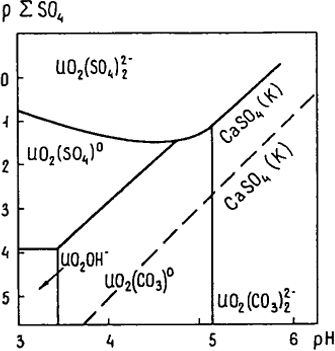
Рис. 3.2. Соотношение полей устойчивости сульфатных и карбонатных комплексных ионов уранила (∑ СО
2 = 1 моль/кг Н
2О,
t = 150°C) (
Наумов, 1978)
Окислительно-восстановительные реакции играют исключительную роль в геохимии урана. Высокая устойчивость U (VI) и низкая устойчивость U (IV) в водных растворах определяют рассеяние урана в одних физико-химических условиях и накопление в других, что в ряде случаев приводит к образованию месторождений. Система U4+ ←→ UО
недостаточно обратима. При отсутствии комплексообразователей и низких (природных) концентрациях урана в водных растворах эта реакция имеет вид
U4+ + 2Н2O ←→ UO
+ 4Н
+ + 2
e-.
Окислительно-восстановительная реакция одного элемента всегда связана с восстановительно-окислительной реакцией другого элемента. Окисление может осуществляться кислородом (О2 → O
+
е-), любым другим анионообразователем и, наконец,
46
ионом, обладающим более высоким окислительно-восстановительным потенциалом.
Для геохимии урана наиболее важной окислительно-восстановительной системой является ассоциация уран - железо. Так, согласно В.В. Щербине (1972), в кислой сульфатной среде реакция
Fe2+ → Fe3+ + е- (Е0 = +0,771 В)
будет окислительной по отношению к реакции
U4+ + 2Н2О → UO
+ 4Н + 2
е- (
Е0 = +0,407 В).
Суммарная реакция будет протекать по схеме
2Fe3 + U4+ + 2Н2О → 2Fe2+ + UO
+ 4Н (
E0 = 0,567 В);
E0 = 0,771 - 0,407 : 2 = 0,567.
В то же время реакция окисления урана является восстановительной для железа.
При переходе от кислой среды к щелочной потенциалы резко меняются, становятся ниже. Так как в реакциях участвует неодинаковое число электронов, то элементы в окислительно-восстановительном ряду часто меняются местами. Так, в щелочной среде система уран - железо будет иметь вид
Fe(OH)2 + ОН1 → Fe(OH)3 + е- (Е0 = -0,56 В),
U(OH)4 + 2(ОН1) → UO2(OH)2 + 2Н2О + 2е (Е0 = -0,49 В).
Так как E
>
E, то 2-я реакция более электроположительна, чем 1-я, и уран является окислителем по отношению к железу. Таким образом, реакция 2Fe
2+ + U
6+ ←
→ 2Fe
3+ + U
4+ в кислой среде идет справа налево, а в щелочной - слева направо.
В реакциях восстановления урана важную роль играет органическое вещество. Восстановителем является либо само окисляющееся органическое вещество, либо восстановленные им H2S или Fe (II). Очень важен состав органического вещества. Предельные углеводороды почти не являются восстановителями. У непредельных углеводородов с двойной связью - С = С - восстанавливающие свойства более проявлены. Наиболее сильно они выражены для оксикислот. Например, при разложении клетчатки образуются соединения группы Сахаров, легко дающие такой сильный восстановитель, как аскорбиновая кислота. С повышением степени углефикации растительных остатков восстановительные свойства ослабевают в ряду: бурый уголь → антрацит → шунгит → графит.
47
