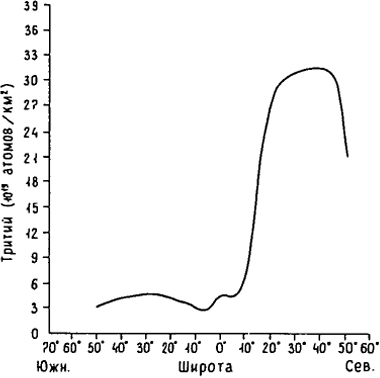
Рис. 11.1. Широтное распределение
3Н на единицу площади в верхнем слое вод Тихого океана до глубины 500 м в 1965 - 1972 гг. (
nо Michel, 1976, из кн.: Источники и действие ионизирующей радиации, 1978)
В океан радионуклиды поступают из атмосферы, с континентальным стоком (включая и непосредственный сброс отходов) и за счет реакторов на атомных судах. Так, тритий, находящийся в атмосфере в составе водяных паров в форме 1Н3НО, легко вступает в реакцию изотопного обмена с поверхностным слоем океанической воды. Концентрация трития в этом слое показана на рис. 11.1. 14С, присутствующий в тропосфере в виде 14СО2, также обогащает океаническую воду в результате изотопного обмена.
255

Рис. 11.2. Колебания избытка
14С в тропосфере и на поверхности океана в 1955 - 1980 гг.
(Источники и действие..., 1978)
Распределение антропогенного 14С в поверхностном слое океанической воды показано на рис. 11.2. Изотопы Sr. Cs. Ce. Ru, Zr, Nb и других нелетучих элементов поступают в атмосферу в форме аэрозолей, среди которых наибольшей растворимостью обладают изотопы Sr.
Один из основных источников загрязнения океана - сброс радиоактивных отходов. Химический состав таких сбросов и формы нахождения в них радионуклидов сильно зависят от принятой на том или ином предприятии технологии. Они могут представлять собой кислые или щелочные растворы, концентрированные растворы солей, содержать в своем составе органические соединения, использовавшиеся в экстракционных процессах. В связи с этим радионуклиды могут находиться в форме комплексных соединений с органическими и неорганическими лигандами (Громов, Спицын, 1975). Например, цирконий может присутствовать в виде устойчивых комплексов с фторид- и оксалатионами. В то же время при низкой кислотности микроконцентрации Zr4+ будут образовывать коллоиды. Nb5+ также легко гидролизуется с образованием коллоидов. Технеций, обладающий несколькими степенями окисления, легко окисляется до валентности +7, образуя анион пертехнетата (ТсО
), характерный для водных сред. Рутений в морской воде, как правило, образует очень устойчивые комплексы. В кислых растворах он находится в виде катионов Ru
3+ и Ru
4+. В щелочной среде для рутения более характерны анионные формы, где он может иметь валентность +5, +6 и +7. Стронций и цезий в жидких сбросах обычно представлены простыми ионами Sr
2+ и Cs
+. Йод активно взаимодействует с органическими экстрагентами, образуя очень устойчивые
256
соединения. Редкоземельные элементы обычно присутствуют в форме гидроксидов (щелочная среда) либо простых или комплексных катионов (кислая среда). Уран, плутоний и торий также находятся в составе очень различных простых или комплексных ионов. Таким образом, с жидкими отходами радионуклиды поступают в океан преимущественно в виде растворимых соединений и сразу же вовлекаются во все физико-химические и биохимические процессы, протекающие в морской среде. При этом одни и те же радионуклиды могут находиться в морской воде в виде различных по составу и растворимости соединений. Они будут сильно отличаться от соединений тех же самых природных элементов (изотопных носителей), растворенных в морской воде.
Выделяют три основные группы радионуклидов, поведение которых в морской воде резко различается (Громов, Спицын, 1975):
- 1) легко растворимые в воде (3Н, Тс, 90Sr, 89Sr);
- 2) эффективно сорбирующиеся на взвеси (редкоземельные элементы, 91Y, 95Zr, 95Nb, 106Ru, частично Pu и другие индуцированные радионуклиды);
- 3) биологически активные радионуклиды (54Mn, 60Co, 55Fe, 63Ni, 51Cr, 65Zn, а также плутоний).
Миграция 1-й группы контролируется циркуляцией водных масс и их перемешиванием, 2-й группы - преимущественно седиментационными процессами, 3-й - поведением биомассы.
Геохимия 90Sr и 137Cs определяется поведением их изотопных и неизотопных носителей: Sr, Са (для 90Sr) и К (для 137Cs). Большая часть 90Sr содержится в хорошо перемешиваемом слое морской воды над термоклиной и лишь около 1% в настоящее время уже перешло в донные осадки. В прибрежных районах и эстуариях концентрации 90Sr по крайней мере в 5 раз выше за счет смыва с суши. Коэффициент накопления 90Sr морскими организмами составляет для водорослей 100, для крабов и омаров - 10, для рыб - 1. Основная часть 137Cs также сосредоточена в поверхностных водах и уменьшается к глубинным зонам примерно в 30 раз. Период полувыведения 137Cs из поверхностного слоя около 17 лет. Коэффициент накопления морскими организмами около 50.
Изотопы плутония не имеют изотопных или неизотопных носителей в морской воде, подобно 137Cs и 90Sr, поэтому они проникают на большую глубину. Более 50% плутония находится ниже термоклины и до 36% сосредоточено в донных осадках. Коэффициент поглощения Pu морскими организмами из воды для водорослей, планктона и ракообразных составляет от 1000 до 3000, а у рыб - от 1 до 10.
257
