Ступенчатой полимеризацией называется процесс образования полимеров путем постепенного присоединения молекул мономера друг к другу с обязательной миграцией в каждом элементарном акте атома или группы атомов. Элементный состав полимера полностью идентичен составу мономеров.
Ступенчатая полимеризация может быть отнесена к поликонденсационным процессам, так как представляет собой последовательность кинетически независимых бимолекулярных реакций. Синтез полимера при этом протекает без выделения низкомолекулярных продуктов реакции.
Ступенчатая полимеризация характеризуется следующими особенностями:
- 1) образующиеся промежуточные продукты устойчивы и могут быть выделены из сферы реакции;
- 2) реакционная способность промежуточных соединений и исходного мономера одинакова;
- 3) каждая стадия роста полимерной цепи протекает с высокой энергией активации;
- 4) ступенчатая полимеризация - обратимый процесс.
Ниже приводятся примеры ступенчатой полимеризации и сополимеризации:
полимеризация формальдегида в присутствии следов воды
- CH2O + H2O → HOCH2OH;
- НОСН2ОН + СН2О → НОСН2ОСН2ОН, и т.д.
полимеризация этиленоксида в присутствии оснований
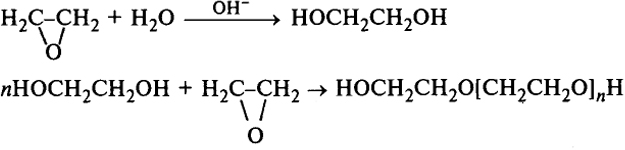
сополимеризация диолов и диизоцианатов с образованием полиуретанов
НО(СН2)4ОН + O=C=N(CH2)6N=C=O → HO(CH2)4OCONH(CH2)6N=C=O;
сополимеризация диаминов и диизоцианатов с образованием полимочевин:
H2N(CH2)6NH2 + O=C=N(CH2)6N=C=O → H2N(CH2)6NHCONH(CH2)6N=C=O.
259
Ступенчатая полимеризация протекает в присутствии гидролитических агентов (воды, кислот, оснований) и поэтому часто называется гидролитической. Вещества, способствующие такому процессу, называются активаторами. Наибольшее значение имеет полимеризация циклов, отличающаяся тем, что в полимере не возникает химических связей иной природы, чем имеющиеся в исходном цикле, а изменяется лишь порядок расположения этих связей в синтезируемой макромолекуле.
Способностью к полимеризации обладают все циклы, имеющие достаточно полярные или способные поляризоваться связи. К их числу относятся циклы, содержащие О, S, N и другие гетероатомы. Склонность циклов к полимеризации связана с напряженностью связей в них. Так, пяти- и шестичленные циклы, как правило, не полимеризуются. Соединения с меньшим и большим числом атомов в цикле способны полимеризоваться. Реакция может быть иллюстрирована следующей схемой:

Если х равно 3 или 4, то реакция сдвинута влево. При количестве метиленовых групп в цикле, большем или меньшем этих значений х, реакция идет с преимущественным образованием полимера. Рассмотрим этот процесс на примере капролактама. Ступенчатая полимеризация состоит из четырех стадий:
1) обратимое расщепление исходного циклического мономера (это самая медленная стадия процесса)
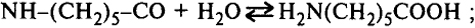
2) зарождение цепи полимера
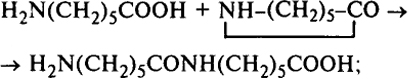
3) рост материальной цепи полимера
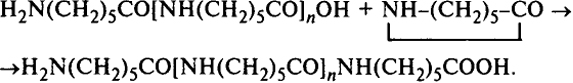
На каждой ступени этого процесса реализуется очередная бимолекулярная реакция. Превращение мономера в полимер продолжается до достижения равновесия.
4) прекращение роста цепи полимера наступает при достижении равновесия.
260
В присутствии воды при полимеризации лактамов протекает два равновесных процесса:
а) гидролиз любой амидной связи внутри макромолекулы (так называемое "амидное равновесие")
CONH~ + Н2О  ~СООН + H2N;
~СООН + H2N;
б) отщепление концевого звена от макромолекулы и превращение его в цикл
~[NH(CH2)5CO]n~ + Н2O  NH-(CH2)5-CO + ~[NH(CH2)5CO]n-1~.
NH-(CH2)5-CO + ~[NH(CH2)5CO]n-1~.
Первая реакция определяет среднюю молекулярную массу полимера, а вторая реакция - его выход.
Таким образом, ступенчатая гидролитическая полимеризация представляет собой сложную систему равновесных реакций синтеза и деструкции, называемую полимеризационным равновесием. С увеличением концентрации активатора скорость полимеризации возрастает, а молекулярная масса снижается. Среднюю степень полимеризации вычисляют по формуле

где Кa - константа амидного равновесия; п - число молей воды, приходящееся на одно элементарное звено полимера.
Для вычисления Ка предложено следующее эмпирическое уравнение:

где Т - абсолютная температура, К.
Когда не применяется никаких активаторов, кроме воды, то
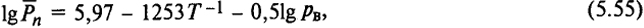
где pв - давление паров воды (Па) при температуре Т.
Задача. Рассчитать среднюю степень полимеризации поликапроамида, полученного при 260°С и содержании воды в системе 1,0 и 1,2% (маc.).
Решение. По формуле (5.54) рассчитаем константу амидного равновесия для температуры 260°С:
lgKa = -0,3 + 1495/533 = 2,500.
Следовательно, Ка = 317.
Вычислим число молей воды, приходящееся на один моль мономера, молекулярная масса которого M0 = 113:
- а) при содержании воды 1,0% (мас.)
- n = 1,0 · 113/(18 100) = 0,063;
- б) при содержании воды 1,2% (мас.)
- n = 1,2 · 113/(18 100) = 0,075.
261
Находим среднюю степень полимеризации Рп по формуле (5.53):
а) Рn = √317/0,063 = 70; Рп = √317/0,075 = 65.
Таким образом, увеличение содержания воды в реакционной среде приводит к уменьшению Рп.
Увеличение концентрации мономеров в реакционной смеси до определенного оптимума приводит к повышению выхода полимера.
Повышение температуры реакции ускоряет процесс полимеризации, но сдвигает полимеризационное равновесие, как и любое другое равновесие, в сторону образования мономерных и олигомерных продуктов.
Задача. Рассчитать необходимую добавку воды для получения полиэнантоамида с молекулярной массой 22000 при 232°С; молекулярная масса мономера М0 = 127.
Решение. Рассчитываем среднюю степень полимеризации:
Рп = 22000/127 = 173.
По формуле (5.54) находим константу амидного равновесия:
lgKa = 0,3 + 1495/505 = 2,66, откуда Кa = 458.
Применяя уравнение (5.53), определим число молей воды, приходящееся на 1 моль энантолактама:
- п = Kа / P = 458/1732 = 0,0153 моль,
- или 100 = 0,21%(мас.)
Таким образом, для получения полиэнантоамида с заданной молекулярной массой необходима добавка воды 0,21 %(мас.).
262
