5.1.3. Ионная полимеризация
Ионной полимеризацией называется процесс синтеза полимеров, при котором активными центрами, возбуждающими цепную реакцию, являются ионы. Ионная полимеризация протекает в присутствии катализаторов. Катализаторы ионной полимеризации можно разделить на три класса:
253
- 1) соединения - доноры протонов: кислоты Бренстенда (HF, НСl и др.) и особенно кислоты Льюиса (АlСl3 + НСl, BF3 + HF и т.д.);
- 2) соединения - доноры электронов;
- 3) катализаторы Циглера - Натта.
Катализаторы первой группы оказываются неэффективными для многих соединений с электроноакцепторными заместителями у двойной связи (стирол, α-винилпирролидон), но они очень активны по отношению к таким веществам, как виниловые соединения с сопряженными связями -С=О и -C≡N.
Катализаторы второй группы способствуют полимеризации виниловых соединений с повышенной электронной плотностью у двойной связи.
Катализаторы Циглера - Натта образуют с молекулой мономера координационный комплекс. Поэтому синтез полимеров в присутствии этих катализаторов называется ионно-координационной полимеризацией.
В зависимости от заряда образующегося иона различают катионную и анионную полимеризацию.
Катионная, или карбониевая, полимеризация протекает с образованием иона карбония - полярного соединения с трехвалентным атомом углерода, несущим положительный заряд. Катализаторами служат вещества, активные в реакциях Фриделя - Крафтса. Катализатор является акцептором, а полимеризующийся мономер - донором электронов:

Анионная, или карбанионная, полимеризация протекает с образованием карбаниона - соединения с трехвалентным атомом углерода, несущим отрицательный заряд. Анионная полимеризация протекает в присутствии доноров электронов - катализаторов второго класса:

Ионная полимеризация ускоряется в присутствии сокатализаторов. При катионной полимеризации сокатализаторами служат
254
гидроксилсодержащие соединения (вода, спирты, кислоты); сокатализаторами полимеризации в присутствии алкилметаллов (катализаторов Циглера - Натта) являются хлориды металлов переменной валентности, например TiCl3. Скорость ионной полимеризации очень велика. Механизм ионной полимеризации включает в себя несколько стадий.
Зарождение (возбуждение) цепи состоит из следующих стадий:
для карбониевого процесса -
1) образование комплексного аниона и протона (кислоты Льюиса)
BF3 + С2Н5ОН  [BF3OC2H5]-H+,
[BF3OC2H5]-H+,
2) активация мономера
Н+ + СН2=С(СН3)2 → СН3 - С+(СН3)2;
для карбанионного процесса -
1) образование аниона
2Na + 2NH3 = 2Na+ + 2NH
+ H
2,
2) активация мономера
NH2 + CH2=CHCN → NH2-CH2-CHCN.
Продолжение (рост) цепи осуществляется путем присоединения мономера к мономер-иону. Регулярное построение макромолекул при последовательном присоединении мономеров "голова к хвосту" определяется полярностью и размером бокового заместителя и ориентирующим действием частиц катализатора.
Протекание процесса ионной полимеризации может быть иллюстрировано следующей схемой:
1) полимеризация с участием свободного иона протекает по схеме
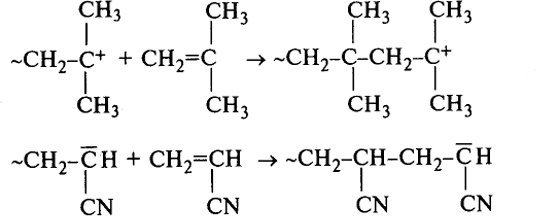
255
2) полимеризация с ионной парой включает следующие этапы цепного процесса:

Ионно-координационная полимеризация. Рост цепи при ионно-координационной полимеризации может проходить:
1) как двухцентровая координационная полимеризация
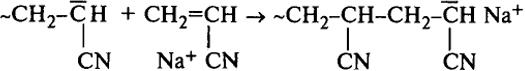
2) как многоцентровая координационная полимеризация (например, с алфиновым катализатором)
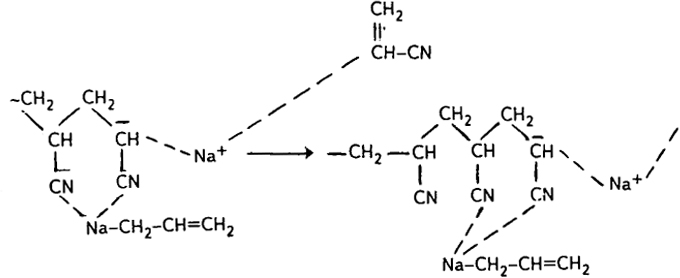
Образование стереорегулярных полимеров при ионно-координационной полимеризации возможно при проведении процесса при низких и даже при повышенной температуре (30-70°С). С увеличением полярности среды скорость процесса и
256
средняя степень полимеризации синтезируемого продукта возрастают.
Обрыв цепи обусловливается следующими реакциями:
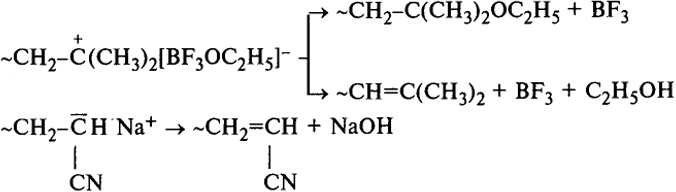
Передача цепи на растворитель может протекать по схеме
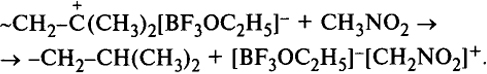
В отличие от радикальной полимеризации константы скорости роста, обрыва и передачи цепи при ионной полимеризации характерны не для того или иного мономера, а только для определенной системы мономер - катализатор - сокатализатор - растворитель, ибо противоион расположен достаточно близко, оказывая существенное влияние на реакции ионизированного конца растущей цепи, а степень ионизации зависит от природы растворителя.
Добавление сокатализатора в количествах, не превышающих стехиометрического соотношения с катализатором, повышает скорость процесса, но снижает степень полимеризации образующегося полимера. Средняя степень полимеризации прямо пропорциональна концентрации мономера и не зависит от концентрации катализатора:

Активный "конец" растущей макромолекулы находится в поле действия противоиона. Вследствие этого каждая новая молекула мономера, приближаясь к растущей цепи, оказывается в поляризующем поле, образованном двумя разноименными зарядами, и, ориентируясь необходимым образом, включается в макромолекулу (макрокатион) в определенном порядке.
Полимеры, полученные в результате ионной полимеризации, отличаются более регулярной первичной структурой, чем при свободнорадикальных процессах.
Задача. Во сколько раз изменится степень полимеризации полистирола при увеличении концентрации стирола с 30 до 80% (мас.) в процессе катионной полимеризации в присутствии серной кислоты?
257
Решение. Согласно уравнению (5.51),
P1 = Kn[М1], P2 = Kn[М2].
Следовательно, при увеличении концентрации стирола степень полимеризации продукта изменится в
Р2/Р1 = [М2]/[М1] = 80/30 = 2,66 раза.
Суммарная скорость ионной полимеризации V прямо пропорциональна концентрации катализатора [Fк]:

Задача. Рассчитать суммарную константу скорости реакции полимеризации стирола в о-ксилоле, если концентрация катализатора - тетрахлорида олова - при 0°С составляла 0,02 моль/дм3; суммарная скорость реакции V = 2,2 · 10-4 дм3/(моль·мин).
Решение. Согласно уравнению (5.52),
К = V/[Fк] = 2,2 · 10-4/0,02 = 1,1 · 10-2 мин-1.
Задача. Рассчитать суммарную константу скорости полимеризации изобутилена в гексане при -78°С, если степень превращения составляла 40 %/ч при концентрации четыреххлористого титана [Fк] = 0,18% и изобутилена [М] = 30.
Решение. Рассчитаем суммарную скорость реакции:
V = 40 · 30/(60 · 100) = 0,2 %/мин.
По формуле (5.52) вычислим суммарную константу скорости реакции полимеризации:
К = 0,22/(0,18 · 60) = 1,8 · 10-2 с-1.
Различие механизмов радикальной, ионной и анионной полимеризации отчетливо проявляется в составе сополимеров, полученных из одной и той же пары мономеров. Значения r1 и r2 (а следовательно, Q и e) изменяются при изменении механизма реакции. Ниже приводятся примерные ряды активности мономеров при ионной сополимеризации:
при карбониевой сополимеризации -
изобутилен > метилстирол > изопрен > стирол > винилацетат > метилметакрилат;
при карбанионной полимеризации -
акрилонитрил > метилакрилат > метилметакрилат > винилацетат > стирол.
258
