2.4.3. Гидродинамические свойства
разбавленных растворов полимеров
Изменение термодинамического качества растворителя, молекулярной массы полимера или температуры раствора вызывает изменение размеров и формы молекулярных клубков. Это приводит к изменению гидродинамических свойств разбавленных растворов полимеров.
Согласно закону Стокса сила сопротивления, которое испытывает сферическая частица при движении в вязкой среде с вязкостью η0, определяется по формуле

где v - средняя скорость движения частиц в растворе.
Движение статистически свернутой в клубок макромолекулы в разбавленном растворе определяется коэффициентом поступательного трения f’:
f’ = F/v.
Для длинных гибких полимерных цепей установлено, что f’ ≈ М
. В этом случае

Для жестких макромолекул принимают

где L - "контурная длина" полимерной цепи.
Макромолекулы, находящиеся в растворе, испытывают гидродинамическое воздействие молекул растворителя, а те в свою очередь - кинетически активных участков полимерных цепей (см. рис. 2.4).
Влияние концентрации полимера на вязкостные свойства его растворов может быть описано некоторым степенным рядом:
ηуд = A0С + A1C2 + А2C3 + ... .
111
В первом приближении эта зависимость определяется как закон Эйнштейна:

здесь ψ - коэффициент формы; для сферической частицы ψ = 2,5, для клубков анизотропной формы

где а и b - большая и малая полуоси гипотетического эллипсоида вращения молекулярного клубка; φ - объемная доля полимера.
Закон Эйнштейна выполняется достаточно строго лишь до концентрации Ск ≤ [η]-1.
При содержании полимера в растворе большем, чем Ск, нарушается линейная зависимость ηуд/C = f(C) вследствие интенсификации межмолекулярных взаимодействий.
Хаггинс показал, что A0 = [η], a A1 = [η]2k'. Для большинства систем полимер - растворитель справедливо следующее уравнение:

Соответствующее разложение в ряд аналогичной зависимости приведенной логарифмической вязкости дает следующее соотношение:

Легко показать, что k’ = 0,5 + β0.
Величина k’ - константа Хаггинса - зависит от молекулярной массы и свойств системы полимер - растворитель и может служить характеристикой интенсивности взаимодействия полимера с растворителем. Значение k’ возрастает с ухудшением термодинамического качества растворителя и уменьшается с понижением температуры.
Судить о степени разветвленности полимера по величине k’ нельзя.
Задача. Рассчитать средневязкостную молекулярную массу Мv и константу Хаггинса k’ для растворов изотактического полипропилена в тетралине при 125°С, если получены следующие значения удельной вязкости:
| С, г/100 см3 |
0,1 |
0,2 |
0,3 |
0,4 |
| ηуд |
0,21 |
0,43 |
0,65 |
0,88 |
Решение. Рассчитываем для каждой концентрации приведенную вязкость ηуд/С : 2,10; 2,15; 2,17; 2,20 и строим график зависимости ηуд/С от С (рис. 2.7). Находим [η] = 2,08 и по уравнению Марка - Хаувинка - Флори (1.32) вычисляем молекулярную массу.
Согласно Приложению 6,
Kη = 0,8·10-4, а α = 0,8; M = 2,08/(0,8·10-4) и Му = 3,56·105.
112
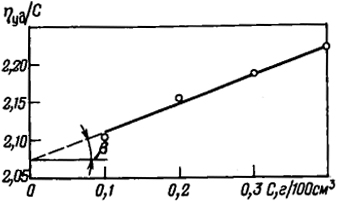
Рис. 2.7. Зависимость приведенной вязкости ηуд/С от концентрации С для растворов изотактического полипропилена в тетралине при 125°С
Из рис. 2.7 находим значение А1 как тангенс угла наклона прямой tgβ:
A1 = tgβ = 0,3, отсюда k’ = A1/[η]2 = 0,3/2,082 = 0,07.
Изменение термодинамического качества растворителя обусловливает соответствующее увеличение или уменьшение коэффициентов разбухания молекулярного клубка ζ.
Как отмечалось ранее, в хороших растворителях ζ > 1. Вычислить [h2]1/2 и η можно из уравнения Флори
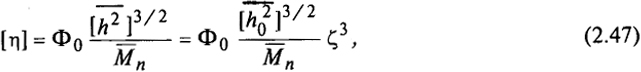
здесь Ф0 - некоторая постоянная, уменьшающаяся от 2,84·1021 в θ-растворителе до 1,60·1021 в хороших растворителях (концентрация раствора выражена в г/100 см3).
Вопрос. При добавлении в диметилформамидный раствор полиакрилонитрила небольших количеств метилового спирта наблюдается снижение характеристической вязкости. Объясните причину этого явления.
Ответ. Метиловый спирт является нерастворителем для полиакрилонитрила. Введение его в диметилформамидные растворы ухудшает термодинамическое качество растворителя, что приводит к свертыванию молекулярных клубков, уменьшению их гидродинамического сопротивления и в результате - к снижению [η].
Так как изменение второго вириального коэффициента В обусловлено теми же факторами, что и изменение ζ, то
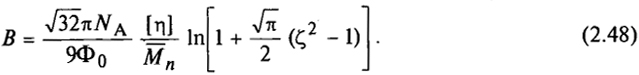
Поэтому в θ-растворителе ζ = 1 и В = 0.
Задача. Рассчитать среднеквадратичное расстояние между концами статистически свернутой макромолекулы полиакрилонитрила в θ-растворителе
113
диметилформамид - метиловый спирт (80:20), если для полимера с Mv = 8·105 [η]θ = 4,23.
Решение. Так как для θ-растворителя ζ = 1 и Ф0, θ = 2,84·1021, то, согласно формуле (2.47),
[h2]3/2 = Mv[η]θ / Ф0, θ = 1,19·10-15;
[h] = 1,12 · 10-10 см2;
[h]1/2 = 1,06 · 10-6 см = 106 нм.
Отметим, что для системы полиакрилонитрил - диметилформамид
Ф0 = 2,72·1021.
Значения ζ могут быть вычислены из значений [η] в данном и в θ-растворителе:

Вопрос. В результате осмометрических исследований кадоксеновых растворов фракционированных препаратов целлюлозы и амилозы было установлено, что значения Мn в обоих случаях идентичны. Однако вискозиметрические измерения показали, что [η] для целлюлозы больше, чем для амилозы. Объясните вероятную причину этого эффекта.
Ответ. Различия в значениях [η] для кадоксеновых растворов целлюлозы и амилозы могут быть объяснены как различной скелетной гибкостью макромолекул сравниваемых полисахаридов, так и различными величинами термодинамического сродства растворителя и полимера, т.е. их равновесной гибкостью.
Задача. Вычислить коэффициент разбухания ζ для поливинилацетата, если в ацетоне [η] = 2,52, а в θ-растворителе - смеси метилпропилкетон - гептан - [η]θ = 0,92.
Решение. В соответствии с уравнением (2.49)
ζ = ([η]/[η]θ)1/3 = 1,4.
Следует отметить, что значения константы Флори в различных растворителях зависят от ζ:

где Ф0, θ - константа Флори для θ-растворителя, равная 2,84·1021.
Задача. Вычислить величину сегмента Куна Lк макромолекул полиакрилонитрила в θ-растворителе при 25°С, если Кη, θ = 8,0·105.
Решение. Согласно уравнениям (1.32) и (2.47) имеем
[η]θ = Ф0, θ [h]3/2Mv = Kη, θ M.
Поэтому

где M0 - молекулярная масса элементарного звена;
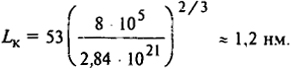
114
Задача. Вычислить [h] макромолекулы с Mv = 5·105, если в некотором растворителе этот полимер характеризуется [η] = 56,8. Значение α = 0,5.
Решение. Если α = 0,5, то полимер растворен в θ-растворителе, для которого ζ = 1. Поэтому
[h] = 56,8·5·105/(2,84·1021) = 1·10-16.
Следовательно, [h]1/2 = 46,4 нм.
Изучение гидродинамических свойств и светорассеяния разбавленных растворов позволяет получить определенную информацию о размерах и форме молекулярных клубков в растворе. Лишь в θ-растворителе макромолекулы приобретают конформацию статистического клубка, в котором взаимное расположение звеньев и сегментов может быть описано вероятностной кривой Гаусса. Тэта-состояния раствора можно достигнуть, либо варьируя соотношение растворитель - осадитель, либо изменяя температуру. Ниже приводятся значения θ-температур (в °С) для растворов полиакрилонитрила в различных растворителях:
| Диметилформамид |
131 |
| Диметилсульфоксид |
96 |
| Азотная кислота 60%-я |
47 |
| γ-Бутиролактон |
107 |
| Гидроксиацетонитрил |
57 |
Например, подбор θ-растворителя методом изменения состава растворяющей смеси основан на определении значения постоянной α в уравнении Марка - Хаувинка - Флори в различных растворителях при изотермических условиях.
Задача. Рассчитать состав растворителя для сополимера акрилонитрила с винилпиридином в θ-точке, если из вискозиметрических данных для его растворов в смеси Диметилформамид - метиловый спирт получены следующие значения:
| ДМФ : СН3ОН, % (об.) |
100:0 |
95:5 |
90:10 |
86:14 |
82:18 |
| α |
0,81 |
0,74 |
0,66 |
0,60 |
0,54 |
Решение. Строим график зависимости а от состава растворителя (рис. 2.8) и при экстраполяции прямой на линию, проведенную через α = 0,5 параллельно оси абсцисс, получаем точку, соответствующую составу θ-растворителя: 80% (об.) диметилформамида + 20% (об.) метилового спирта.
Размеры макромолекулярных клубков можно определить также по интенсивности рассеяния света частицами под одинаковыми углами θ для различных длин волн λ (по дисперсии светорассеяния), если воспользоваться следующим уравнением:
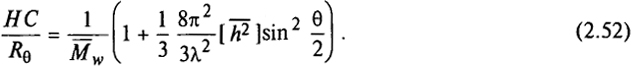
115
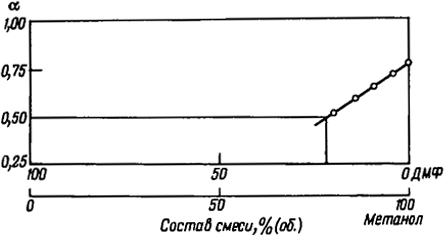
Рис. 2.8. Зависимость а от состава растворитель-осадитель (система полиакрилонитрил-диметилформамид-метанол) при 25°С
Вопрос. Объясните, почему в хороших растворителях значение HC/Rθ для эквиконцентрированных растворов больше, чем в θ-растворителе.
Ответ. Так как величина HC/R0 связана со статистическим размером молекулярного клубка, то ухудшение термодинамического качества растворителя (уменьшение [h2] при Mw = const) влечет за собой ее снижение.
Из сопоставления уравнений (2.48) и (1.58) становится очевидным, что величина HC/τ зависит от значений второго вириального коэффициента В. Если размер молекулярного клубка соизмерим с длиной волны падающего света или больше ее [≥(λ/20)], то возникает асимметрия рассеянного света [см. уравнение (2.49)J.
Так, по графику двойной экстраполяции (по Зимму) можно, оценивая tgφ (см. рис. 1.20), определить В, так как

Из этого же графика может быть определен и радиус инерции молекулярного клубка:
[r2] =
,
где n0 - показатель преломления растворителя; h’ - величина отрезка от начала координат.
Для свободносочлененной цепи [r2] = (1/6)[h2], а для жесткой цепи (для f0 < 0,63) [r2] = (1/12)L2.
Однако достоверная оценка размеров частиц этим способом возможна в двух случаях:
1) при получении на кривой HC/Rθ = f[sin2(θ/2) + КС] не менее 4-5 экспериментальных точек в области
(8/3)π2(h2)/λ2)sin2(θ/2) < 1,
116
что реализуется при ([h2]/λ2)1/2 < 0,7, т.е. при размерах молекулярных клубков < 120 нм;
2) при получении на кривой HC/Rθ = f[sin2(θ/2) + KC] не менее 4-5 экспериментальных точек в области
(8/3)π2([h2]/λ2)sin2(θ/2) > 6,
что реализуется при ([h2]/λ2)1/2 > 0,7, т.е. при размерах молекулярных клубков > 250 нм.
117
