2.3.3. Расчет растворимости полимеров по Аскадскому
Этот подход к оценке растворимости полимеров заключается в следующем. Структура полимеров определяется на молекулярном уровне конформациями, конфигурацией и способами взаимной упаковки макромолекул. Действующий объем атома каждого вида зависит от его окружения, т.е. от природы валентно-связанных с ним атомов и от коэффициентов упаковки молекул вещества, в которые входит данный атом.
Коэффициент молекулярной упаковки может быть оценен из соотношения

где ΔVi - ван-дер-ваальсовы объемы атомов i-го вида; К - коэффициент упаковки.
Для энергии когезии можно аналогично записать, что
KΔE0 = ΔE*.
96
Здесь ΔЕ* представляет собой энергию когезии жидкости, уменьшенную во столько раз, во сколько ван-дер-ваальсов объем молекулы меньше мольного объема. Значение ΔЕ* - величина аддитивная. Поэтому
ΔE* =
Δ
E,
где ΔE - вклад каждого атома и типа межмолекулярного взаимодействия в ΔE*.
Тогда

где NA - число Авогадро.
Значения ΔЕ
приведены в табл. 2.3. Значения Δ
Vi для некоторых атомов в зависимости от их окружения приведены в Приложении 8.
Инкремент объема ΔVi рассматриваемого атома вычисляется как объем сферы этого атома за вычетом объема шаровых сегментов, отсекаемых на этой сфере соседними валентно-связанными атомами, т.е.
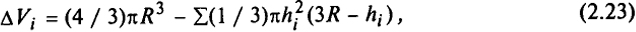
где R - ван-дер-ваальсов радиус рассматриваемого атома; Ri - высота сегмента, которая вычисляется по формуле

где di - длина связей между двумя атомами; Ri - ван-дер-ваальсовы радиусы соседних с рассматриваемыми валентно-связанных атомов.
Задача. Рассчитать параметры растворимости полиакрилонитрила, диметилформамида и диметилсульфоксида. Установить, растворяется ли полимер в этих растворителях.
Решение 1. Рассчитываем параметр растворимости полиакрилонитрила в соответствии с формулой (2.22). Дня элементарного звена полимерной цепи -CH2-CHCN- по табл. 2.3 имеем
ΔE = 3ΔE + 3ΔE + ΔE + 3ΔE = 4623,2 кал/моль
и из Приложения 8
ΔV = ΔVC,7 + ΔVC,4 + ΔVC,43 + 3ΔVH,54 + ΔVN,74 = 54,0 Å3.
Так как NA = 6,06·1023, то
δп = [4623,2/(6,06·1023·54·10-24)]0,5 = 11,9 (кал/см3)0,5.
97
Таблица 2.3. Значения ΔЕ* для различных видов атомов и типов межмолекулярного взаимодействия

Примечания: 1) ΔE вводится при наличии двойных связей, не входящих в состав полярных групп; 2) 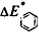 вводится при наличии ароматических ядер с числовым коэффициентом, соответствующим числу этих ядер; 3) ΔE вводится во всех случаях при наличии полярной группы любого типа; в случае хлорированных соединений (при наличии двух и более атомов Сl, присоединенных к одному и тому же углероду) необходимо вводить 2 ΔE; 4) ΔЕ вводится при расчете δ для биполярных апротонных растворителей амидного типа, при этом обычно диполь-дипольное взаимодействие за счет полярных групп учитывается введением соответствующего количества инкрементов ΔE; 5) то же относится к инкременту ΔE, но для апротонных растворителей типа ДМСО; 6) ΔE вводится при наличии водородной связи любого типа; 7) ΔE=CCl2 учитывает специфическое взаимодействие группы =ССl2, при этом ΔE не вводится; 8) ΔE и учитывает проявление полярности в напряженных 3-5-членных циклах, содержащих атом О; 9) ΔE вводится при переходе от нормальных углеводородов к разветвленным.
вводится при наличии ароматических ядер с числовым коэффициентом, соответствующим числу этих ядер; 3) ΔE вводится во всех случаях при наличии полярной группы любого типа; в случае хлорированных соединений (при наличии двух и более атомов Сl, присоединенных к одному и тому же углероду) необходимо вводить 2 ΔE; 4) ΔЕ вводится при расчете δ для биполярных апротонных растворителей амидного типа, при этом обычно диполь-дипольное взаимодействие за счет полярных групп учитывается введением соответствующего количества инкрементов ΔE; 5) то же относится к инкременту ΔE, но для апротонных растворителей типа ДМСО; 6) ΔE вводится при наличии водородной связи любого типа; 7) ΔE=CCl2 учитывает специфическое взаимодействие группы =ССl2, при этом ΔE не вводится; 8) ΔE и учитывает проявление полярности в напряженных 3-5-членных циклах, содержащих атом О; 9) ΔE вводится при переходе от нормальных углеводородов к разветвленным.
98
2. Рассчитываем параметр растворимости диметилформамида

ΔE = 3ΔE + 7ΔE + ΔE + 3ΔE + ΔE + ΔE = 6579 кал/моль.
В некоторых случаях для определения инкремента объема атома нет табличных данных. Тогда его можно рассчитать по следующей схеме. Например, необходимо определить инкремент объема атома углерода, обрамленного следующими атомами  , отличающегося от атома углерода в комбинации 41 (см. Приложение 8) тем, что к нему присоединен атом водорода, а не углеродный атом. Оценим, как изменится искомый объем при замене замещающего атома углерода на атом водорода. Изменение объема можно рассчитать из разности значений ΔVC,1 и ΔVC,4, где ΔVC,1 и ΔVC,4 - величины, приведенные в Приложении 8. Имеем
, отличающегося от атома углерода в комбинации 41 (см. Приложение 8) тем, что к нему присоединен атом водорода, а не углеродный атом. Оценим, как изменится искомый объем при замене замещающего атома углерода на атом водорода. Изменение объема можно рассчитать из разности значений ΔVC,1 и ΔVC,4, где ΔVC,1 и ΔVC,4 - величины, приведенные в Приложении 8. Имеем
ΔV = ΔVC,4 - ΔVC,1 = 9 - 5 = 4Å3.
Следовательно, инкремент объема искомого атома углерода будет равен ΔVC,41 + 4Å3 = 14,3 + 4 = 18,3 Å3. Аналогично рассчитываем ΔV атома углерода в группе NСН3 по ΔVC,37:
ΔV = 14,6 + 4 = 18,6 Å3;
∑ ΔV = ΔV + ΔV + ΔVH,54 + ΔVO,55 + ΔVN,68 = 76,25 Å3.
Отсюда
δр = [6579,6/(6,06·1023·76,25·10-24)]0,5 = 11,9 (кал/см3)0,5.
3. Рассчитываем параметр растворимости диметилсульфоксида
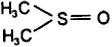
ΔE = 2ΔE 6ΔE + ΔE + ΔE + ΔE + ΔE = 7503 кал/моль;
ΔV = 2ΔVC,44 + ΔVS,75 + 6ΔVH,54 + ΔVO,65 = 70,1Å3;
δр = [7503/(6,06·1023·70,1·10-24)]0,5 = 13,3 (кал/см3)0,5.
Полиакрилонитрил растворим как в диметилформамиде, поскольку 11,9 - 11,9 = 0, так и в диметилсульфоксиде, так как 13,3 - 14,9 = 1,4, что меньше 2,0 (кал/см3)0,5.
99
Для сополимера или смеси двух растворителей параметры растворимости вычисляются из соотношения

где α1 - мольная доля компонента 1 в сополимере или доля жидкости 1; ( ΔE)1 и ( ΔE)2 - эффективные энергии когезии компонентов 1 и 2 в сополимере или жидкостей 1 и 2; ( ΔVi)1 и ( ΔVi)2 - ван-дер-ваальсовы объемы компонентов.
Задача. Рассчитать параметры растворимости сополимера акрилонитрила (АН) и винилхлорида (ВХ) в соотношении 40:60% (мас.) и ацетона. Растворим ли этот волокнообразующий сополимер в ацетоне?
Решение. Формулу сополимера запишем в виде
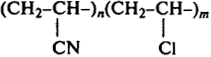
Рассчитываем мольные доли компонентов. В сополимере содержится 40/53 моль АН и 60/62,5 моль ВХ.
Тогда
α1 = = = 0,44.
Из предыдущей задачи для ПАН имеем
( ΔE)1 = 4623,2 кал/моль.
Рассчитываем эту характеристику для ПВХ:
( ΔE)2 = 2ΔE + 3ΔE + ΔE + ΔE = 2644,8 кал/моль;
( ΔVi)2 = ΔVC,7 + ΔVC,51 + 3ΔVH,54 + ΔVCl,81 = 13,1 + 10,1 + 3 · 2 + 19,85 = 49,05 Å3;
Следовательно,
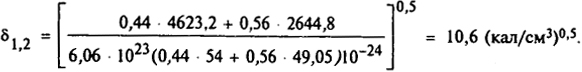
Рассчитываем параметр растворимости ацетона  :
:
ΔE* = 3ΔE + 6ΔE + ΔE + ΔE = 3·550,7 + 8·47,7 + 142,6 + 1623 = 3703,9 кал/моль;
100
ΔV = 2ΔVC,10 + ΔVC,32 + ΔVО,55 + 6ΔVH,54 = 2·17,2 + 12,8 + 5,85 + 6·2 = 65,05 Å3;
δр = [3703,9/(6,06·1023·65,05·10-24)]0,5 = 9,7 (кал/см3)0,5.
Так как δ1,2 - δр = 10,6 - 9,7 = 0,9, т.е. меньше 2,0, то сополимеры АН (40%) и ВХ (60%) могут растворяться в ацетоне.
101
