2.3.1. Взаимодействие растворителей с полимерами
Растворы большинства высокомолекулярных соединений, как было сказано, являются истинными. Однако значительные молекулярные массы и полидисперсность обусловливают нарушение термодинамической обратимости их свойств уже при малых концентрациях. Отличительной особенностью процесса растворения является набухание, предшествующее собственно растворению. В зависимости от первичной структуры полимера (наличия и природы боковых заместителей в звеньях полимерной цепи, регулярности строения макромолекулы) набухание может быть ограниченным и неограниченным, т.е. завершающимся образованием раствора.
При смешении полимера и растворителя наблюдается изменение суммарного объема раствора (контракция) ΔVк. Если vп и vp - парциальные мольные объемы полимера и растворителя соответственно, а ΔV = Vт - Vэ, где Vт и Vэ - теоретический (расчетный) и экспериментально определенный (фактический) объемы смеси, то

Для полимеров специфично явление ограниченного набухания. Взаимодействие полимера и растворителя является диффузионно-контролируемым процессом: проникновение молекул растворителя в полимерный субстрат приводит к постепенному
90
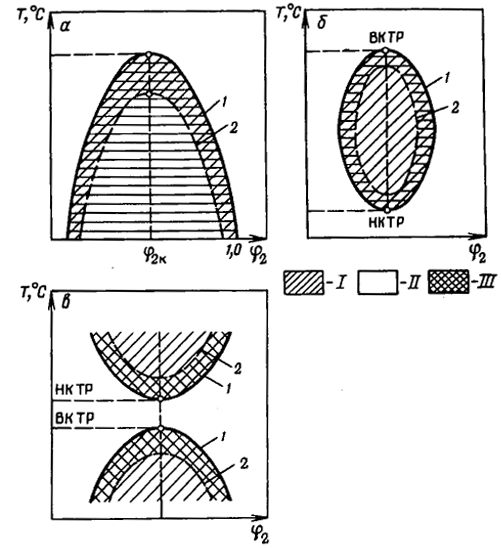
Рис. 2.3. Фазовые диаграммы состояния растворов полимеров состав - температура:
а: ΔHсм > 0, ΔSсм > 0; б: ΔHсм > 0, ΔSсм < 0; в: ΔHсм < 0, ΔSсм < 0; 1 - бинодаль; 2 - спинодаль; I - двухфазная область; II - однофазная (гомогенная) область; III - метастабильная область
разрыву межмолекулярных связей между цепями и образованию новых, сольватационных контактов между растворителем и полимером.
Предельная растворимость может быть достигнута изменением температуры раствора и состава растворителя. При изменении этих факторов полимер может и терять растворимость, что визуально проявляется в помутнении раствора. Температура, при которой становится возможным визуальное определение мутности, называется температурой осаждения, Тo.
Температура осаждения данного полимера в данном растворителе как функция объемной доли растворенного вещества может быть представлена фазовыми диаграммами (рис. 2.3).
Область истинного раствора от области начала помутнения раствора (начала осаждения) отделяется кривой, называемой бинодалью. Но распад раствора на различные фазы происходит не скачкообразно, а постепенно. Эта переходная область называется
91
областью метастабильного состояния и ограничивается переходом в двухфазное состояние. Кривая, условно разделяющая эти две области, называется спинодалью. Максимумы и минимумы на бинодалях называются соответственно верхняя (ВКТР) и нижняя (НКТР) критические температуры растворения.
Различные системы волокнообразующий полимер - растворитель могут иметь совершенно непохожие фазовые диаграммы.
Растворение протекает самопроизвольно лишь в тех случаях, когда процесс сопровождается уменьшением свободной энергии системы. Изменение этого термодинамического параметра системы полимер - растворитель определяется вторым законом термодинамики:

где ΔGсм, ΔHсм и ΔSсм - изменение свободной энергии, энтальпии и энтропии растворения соответственно (индекс "см" означает "смешение").
Типы фазовых диаграмм определяются термодинамическими параметрами.
При ΔHсм > 0 и ΔSсм > 0 диаграмма состояния имеет вид, показанный на рис. 2.3, а, и характеризуется ВКТР (например, система триацетат целлюлозы - хлороформ, полистирол - циклогексан). При ΔHсм < 0 и ΔSсм < 0 на диаграмме состояния появляется точка НКТР. Такие диаграммы характерны для многих волокнообразующих полярных полимеров: полиакрилонитрил - диметилформамид, поливиниловый спирт - вода. В некоторых случаях фазовая диаграмма имеет вид, подобный приведенному на рис. 2.3, б.
Сольватационное взаимодействие макромолекул и молекул растворителя существенно изменяет способность полимерных цепей к конформационным переходам, т.е. влияет на их равновесную гибкость. По величине термодинамического сродства к полимеру все растворители делятся на "хорошие" и "плохие". Для термодинамически "хороших" растворителей характерно образование достаточно мощных сольватных оболочек вокруг макромолекул, что существенно уменьшает возможность их конформационных переходов, т.е. обусловливает снижение равновесной гибкости.
В "хороших" растворителях размеры молекулярных клубков увеличиваются, что приводит к изменению их гидродинамических свойств, а количество кинетически независимых частиц, в роли которых выступают сегменты макромолекул, снижается. Это влечет за собой изменение количественных характеристик растворов полимеров.
92
В термодинамически "плохом" растворителе внутреннее взаимодействие преобладает над сольватационным, и макромолекула стремится свернуться в сравнительно плотный клубок. Растворитель, в котором взаимное расположение элементарных звеньев полимерной цепи в статистическом клубке может быть описано вероятностной кривой Гаусса, называется тэта-растворителем (θ-растворитель). Вместе с тем температура, при которой взаимодействие между полимером и растворителем отсутствует, называется тэта-температурой (θ-температура). Небольшое снижение температуры раствора ниже θ-температуры, а также незначительная добавка осадителя к раствору полимера в θ-растворителе вызывает начало разделения раствора на фазы, т.е. осаждение полимера. ВКТР соответствует θ-температуре раствора полимера, обладающего бесконечно большой молекулярной массой.
93
