Осмометрия
При растворении полимера происходит уменьшение химического потенциала растворителя в растворе μ1 по сравнению с его величиной в чистом растворителе μ
. Это обусловливает одностороннее движение частиц растворителя в раствор через полупроницаемую перегородку, разделяющую раствор и чистый растворитель. Разбавление раствора прекращается, когда активность молекул растворителя по обе стороны мембраны становится одинаковой. Это может быть достигнуто только при бесконечно большом разбавлении. При этом объем раствора увеличивается, что влечет за собой соответствующее повышение гидростатического давления. Такое равновесное гидростатическое давление эквивалентно осмотическому.
Если πo - осмотическое давление, то в соответствии с уравнением Вант-Гоффа

где п - число молей вещества; V - объем раствора.
Таким образом, πo, являясь коллигативной характеристикой раствора, зависит только от числа частиц и не зависит от строения растворенного вещества и растворителя:

где а0 - активность растворителя.
С другой стороны,

где Сi - массовая концентрация растворенного вещества.
27
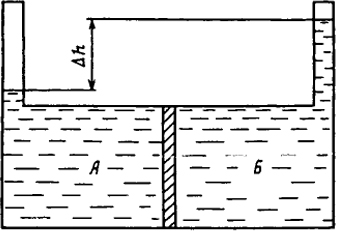
Рис. 1.6. Принципиальная схема осмометра. Пояснения в тексте
Сопоставляя уравнения (1.7) и (1.18), видим, что
πo = -(μ1 - μ
)/
V1,
т.е. величина осмотического давления однозначно характеризует изменение химического потенциала раствора при изменении его концентрации.
Принципиальная схема осмометра приводится на рис. 1.6. Сосуд, снабженный двумя одинаковыми капиллярами, разделен мембраной, которая способна пропускать только молекулы растворителя. В отсек А наливают растворитель, а в отсек Б - испытуемый раствор. Осмометр тщательно термостатируют. В результате осмоса объем жидкости в отсеке Б увеличивается до тех пор, пока гидростатическое давление столба жидкости в капилляре отсека Б не уравновесит величину осмотического давления.
Подставляя значения п из уравнения (1.20) в уравнение (1.18), получаем

или для полидисперсного продукта
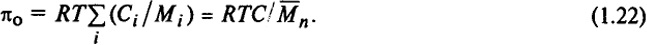
Уравнение (1.18) применимо к идеальным системам, где взаимодействием между растворенными частицами можно пренебречь.
При переходе к реальной системе приходится учитывать возможные контакты между макромолекулами, что математически можно описать некоторым степенным рядом. Для изменения химического потенциала раствора справедлив следующий ряд:

Соответственно для осмотического давления

28

Рис. 1.7. Зависимость πo/С = f(С) для растворов:
1 - в термодинамически хорошем растворителе; 2 - в θ-растворителе
Такие уравнения называются вириальными, а коэффициенты В, D и последующие - вириальными коэффициентами.
Осмотические свойства разбавленных растворов полимеров в большинстве случаев удовлетворительно описываются вириальным уравнением с двумя первыми членами:

Уравнение (1.25) графически изображается прямой с тангенсом угла наклона tgα = RTB/Mn, после экстраполяции отсекающей на оси ординат отрезок, равный RT/Мn (рис. 1.7).
Величина πo/C называется приведенным осмотическим давлением; величина RT/Мп = [πo/СlC→0] = [π] - характеристическим осмотическим давлением (концентрация раствора С выражается в г/см3).
Следовательно, по результатам измерений осмотического давления молекулярная масса Мп полимера может быть вычислена из уравнения

где Т - абсолютная температура, К; R - универсальная газовая постоянная, R = 82,06 см3·атм/(град·моль) = 8,314 Дж/(град·моль).
Обычно осмотическое давление одновременно определяют в 4-5 осмометрах, помещенных в один термостат, при различных концентрациях раствора.
Для определения молекулярной массы осмометрическим методом применяют два способа: "статический", когда измеряется
29
равновесная разность уровней в осмометре, и "динамический", когда измеряется скорость проникновения растворителя через мембрану в зависимости от приложенного давления. В случае полимеров, растворимых в органических растворителях, обычно используют в качестве полупроницаемой мембраны пленку бактериальной целлюлозы, свежеформованный целлофан, а также поливинилспиртовую пленку.
Величину осмотического давления оценивают по измерению высоты столба жидкости в капилляре Δh (см. рис. 1.6). Если ρ - плотность раствора (практически равная плотности растворителя), то πo (в Па) можно вычислить по формуле

Вопрос. Объясните возможную причину завышенных значений Мп, получаемых при использовании долго хранимых пленок-мембран.
Ответ. Одной из возможных причин получения завышенных значений Мп при использовании мембран после длительного хранения является их старение, т.е. релаксационное уплотнение структуры, приводящее к понижению проницаемости пленки.
Задача. Рассчитать среднечисленную молекулярную массу и степень полимеризации поли-α-метилстирола, если при измерении осмотического давления при температуре 25°С для его растворов в толуоле получены следующие данные:
| С·102, г/см3 |
0,30 |
0,50 |
0,78 |
0,98 |
| Δh, мм |
0,98 |
1,65 |
2,83 |
3,75 |
Плотность толуола ρ = 0,8623 г/см3.
Решение. Вычисляем осмотическое давление πo по формуле (1.27), а затем отношение πо/С, принимая во внимание, что С выражена в г/см3:
| πo·103, атм |
0,80 |
1,38 |
2,36 |
3,13 |
| πo/С |
0,27 |
0,28 |
0,30 |
0,32 |
Аналитическое решение зависимости πo/С = от С выражается уравнением прямой линии зависимости πo/С = 0,24 + 8,062С (при этом σ2 = 6,86·10-6), в соответствии с которым (πo/C)C→0 = [π0] = 0,24.
Согласно формуле (1.26)
Мn = 82,06(273 + 25)/0,24 = 102000;
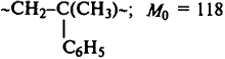
Pn = 102000/118 = 860.
Точность измерения осмотического давления πo зависит от правильности выбора мембраны. Осложняющими факторами являются:
- а) "асимметрия мембраны" - разность уровней поднятия столба растворителей в обеих камерах осмометра, возникающая вследствие неоднородности структуры пленки;
30
- б) значительная адсорбция макромолекул полимера из раствора поверхностью мембраны, приводящая к уменьшению числа частиц.
Применение структурно-однородных мембран на основе бактериальной целлюлозы, а также изотропных поливинилспиртовых пленок позволяет существенно уменьшить ошибку измерения осмотического давления, а следовательно, и молекулярной массы.
Вопрос. Объясните, почему невозможно определить осмометрическим методом Мn полиакролеина, растворимого в диметилформамиде, при использовании целлюлозных или поливинилспиртовых мембран?
Ответ. Основной причиной, препятствующей правильному определению Мn этого полимера осмометрическим методом, является взаимодействие между ОН-группами полимерного субстрата мембраны и сорбируемыми на ней макромолекулами полиакролеина.
Возможности определения молекулярной массы осмометрическим методом ограничиваются точностью отсчета Δh, а также проницаемостью мембраны для частиц исследуемого вещества. Наиболее достоверные значения Мп, получаемые методом осмометрии, находятся в пределах от 1·104 до 7·105.
31
